25 Abr Hemoglobina
La hemoglobina (Hb) es una hemoproteina, es decir, una proteína al que tiene unido un grupo especializado prostético nombrado grupo hemo. Su conjunto da como resultado una molécula aproximadamente esférica que se encuentra en los eritrocitos, donde su función principal es transportar oxígeno (O2) desde los pulmones a todos los tejidos del cuerpo (Mckee&Mckee, 2003).
La Hb es un tetrámero formado por cuatro cadenas polipeptídicas de tipo globular. La combinación de éstas, dispuestas en dos dímeros idénticos, resultará en diferentes tipos de Hb. La más representativa es la Hb del adulto, llamada HbA1 (figura 1), conformada por dos cadenas tipo α y dos tipo β (α2β2), cada una con una estructura primaria (secuencia de aminoácidos) diferente. También se ha descrito una Hb fetal (HbF) conformada por α2γ2 γ otra Hb del adulto (HbA2, mucho menos frecuente que la anterior) conformada por α2δ2. Cada una de las cadenas está unida a un grupo hemo, albergando así un total de cuatro grupos por cada molécula de Hb.
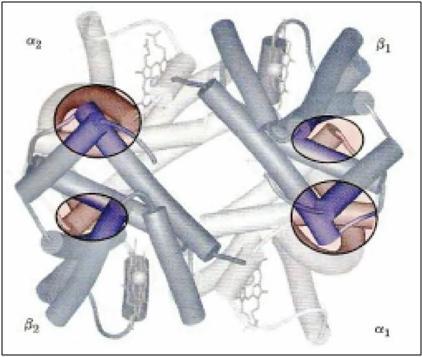
Figura 1. Estructura tridimensional de la HbA1 (extraído de Nelson&Cox, 2005).
Las configuraciones tridimensionales de la mioglobina y de las cadenas α y β de la HbA1 con el grupo hemo son muy semejantes, aunque sus secuencias de aminoácidos son diferentes. Por esa razón se sugiere al lector la lectura del término mioglobina para profundizar con más detalle entre la interacción del grupo prostético hemo, el átomo de hierro fijado en su estructura y su relación con
el oxígeno.
Así entonces, tanto la mioglobina como la Hb poseen la capacidad de unir O2 de forma reversible, pero ésta última, al tener una estructura más compleja, sus propiedades de unión son más complicadas (Mckee&Mckee, 2003). Al poseer cuatro grupos hemo tiene la capacidad de unir cuatro moléculas de O2. La unión del primer oxígeno produce un serie de cambios a nivel estructural entre los dímeros que potencia la unión de un nuevo oxígeno en la misma molécula (fenómeno llamado unión cooperativa). De esta forma la curva de disociación de la Hb presenta una forma sigmoidea, a causa de sus modificaciones estructurales que facilitan o dificultan la saturación o la disociación en función del estado (desoxiHb u oxiHb) que presenta la molécula y la presión de oxígeno al que esté sometida (Figura 2).
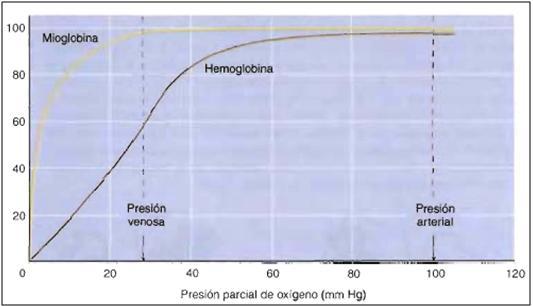
Figura 2. Curva de disociación de oxígeno en la mioglobina y la hemoglobina (extraído de Mckee&Mckee, 2003). La forma sigmoidea de la Hb es trascendental, ya que nos aseguran que
pequeñas variaciones en las presiones parciales de oxígeno aún saturarán la Hb pudiendo así cumplir con sus funciones de reparto de O2. Imagínense que en lugar de una curva sigmoidea la Hb siguiese un crecimiento lineal, en situaciones de gran altitud, donde las presiones parciales de O2 son mucho menores (hipoxia), la Hb no sería capaz de saturarse y las consecuencias serían nefastas, incapacitando ya no sólo la realización de ejercicio, sino incluso el estado de reposo.
El transporte de O2 en la sangre se ve influido por la presión de dióxido de carbono (CO2), el pH (H+) y la temperatura. Todos estos factores están aumentados en la musculatura local en condiciones de ejercicio, favoreciendo la cesión de O2 desplazando la curva de disociación hacia la derecha, es decir favoreciendo el estado desoxiHb y por lo tanto facilitando la adaptación del organismo a las nuevas demandas aumentadas a causa del ejercicio. La influencia que ejerce el CO2 y la disminución del pH sobre el O2 se conoce como efecto Bohr, y en caso inverso, efecto Haldane. El primero indica que la mayor concentración de CO2 en los músculos activos favorece la liberación de O2 por parte de la
Hb; el segundo indica todo lo contrario, situación dada en los tejidos pulmonares, donde las altas presiones de O2 favorecen la eliminación de CO2.
De todo esto se deduce que la Hb aparte de su función como transportadora de O2, también tiene la capacidad para trasportar CO2 y liberarlo en los pulmones, aunque no sea su principal función (transporta un 20% aproximadamente del total de CO2 generado), ya que hay otros potentes mecanismos de eliminación de éste,como es su reacción con el agua que se da dentro del eritrocito, gracias a presencia de la anhidrasa carbónica, que permite transformarlo en bicarbonato (HC03) y H+. El HC03 es expulsado de los eritrocitos hacia el plasma, fenómeno que conlleva una disminución del pH sanguíneo. De manera simultánea se da la unión delos H+ a varios grupos ionizables en las moléculas de Hb, este mecanismo potencia la disociación del O2, favoreciendo el estado desoxiHb (Mckee&Mckee, 2003).
Un último componente que altera la función de transporte de O2 de la Hb es el 2,3-bisfosfoglicerato (BPG), substancia formada en los eritrocitos por una vía colateral a la glucólisis a en situaciones de hipoxia (Barbany, 2002). Una molécula de BPG cargada negativamente se une en una cavidad central dentro de la hemoglobina que está alineada con aminoácidos con carga positiva (Mckee&Mckee, 2003), induciendo de nuevo el estado desoxiHb. Todos estos mecanismos que favorecen la liberación del O2, necesarios para mantener las demandas metabólicas y de esta manera favorecer la continuidad del ejercicio, se resumen en la Figura 3.
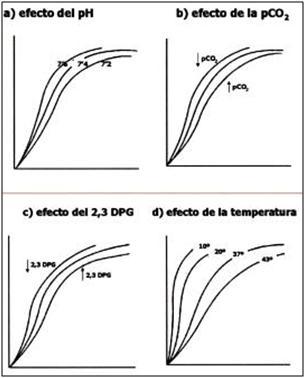
Figura 3: Factores que influyen sobre la curva de transporte de O2 por la Hb (extraído de Barbany, 2012).
Uno de los factores determinantes del rendimiento deportivo en los deportes de resistencia es el consumo máximo de oxígeno (VO2máx). Éste está limitado por la capacidad del sistema cardiorrespiratorio de transportar el oxígeno a los músculos que se están ejercitando. Se ha determinado que es el transporte de O2, y no la extracción de O2 por el músculo esquelético, el principal limitante del VO2máx en los humanos (Bassett&Howley, 2000). El O2 es transportado por la sangre en combinación con la Hb (>98%) o disuelto en ella (>2%) (Willmore&Costill, 2007). De esta forma al alterar los mecanismos involucrados en el transporte de O2 se puede intuir una modificación del rendimiento deportivo.
Una de las adaptaciones del entrenamiento de resistencia es un aumento en las concentraciones de glóbulos rojos (y por lo tanto de Hb, presentes en éstos) que la correspondiente a persona sanas de la misma edad, superficie corporal y sexo. Se plantea que este efecto obedece a una situación de flujo reducido de O2 a los tejidos “sensores” y éstos ejecutarán una orden compensatoria para reparar dicha situación. El razonamiento tiene lógica ya que en efecto, uno de les tejidos que más ve reducido su flujo durante el ejercicio es el renal (Calderón, 2007). El riñón aumentará la producción de eritropoyetina (EPO), que es la hormona encargada de aumentar la producción de glóbulos rojos. Éste mismo efecto sobre la inducción de la EPO es lo que buscan entrenadores y deportistas al someterse a entrenamientos en altitud durante periodos relativamente prolongados, o a través de protocolos de entrenamiento en hipoxia intermitente. Estos métodos se basan en generar esa hipoxia al mecanismo sensor a través de la en inspiración de una atmósfera con baja presión de O2 o con una mezcla de gases con poca cantidad de oxigeno.
Otra forma poco ética y prohibida de obtener estos beneficios, pero utilizada por algunos deportistas, es a través del dopaje. Hay dos mecanismos principales por los cuales se puede aumentar el número de glóbulos rojos. El primero es a través del dopaje sanguíneo y básicamente se trata de reducir la concentración de eritrocitos a través de una extracción de sangre, la cual el organismo responderá compensando esta falta de sangre (éste proceso no es inmediato), a su estado basal (a través del mismo mecanismo de la producción endógena de EPO), momento en el que se trasfunde la sangre extraída anteriormente y de esta forma contar con un mayor número de eritrocitos que en un inicio. El segundo mecanismo es a través del doping hormonal, administrando EPO farmacológica de manera exógena para potenciar sus efectos beneficioso sobre el transporte de O2 ya comentados. Ha pesar de la pobre imagen y el castigo que han sufrido varios deportistas exitosos, éste tipo de prácticas aún son bastante recurrentes en el mundo del deporte profesional y
amateur.
Finalmente, pueden darse diversas situaciones que pueden provocar un decremento del rendimiento si no se tiene clara esta relación positiva entre eritrocitos/Hb y desempeño deportivo. Un ejemplo de ello ocurre con la donación de sangre, la extracción es de aproximadamente unos 500ml, aproximadamente entre un 8-10% del volumen total de sangre con su reducción paralela de eritrocitos. Se necesitarán al menos unas 6 semanas para reconstituir el número de glóbulos rojos ya que deben desarrollarse plenamente antes de resultar funcionales (Willmore&Costill, 2007). Esto supondrá una bajada de rendimiento del deportista por afectación a la capacidad de transporte de O2. Lo mismo puede suceder en caso de desarrollar una anemia (Hb inferior a rangos establecidos como normales), y aquí entra la importancia de llevar junto a un control de las cargas de entrenamiento, un control bioquímico del deportista, que puede explicar el porque de una bajada en el rendimiento al ver una Hb inferior a los valores de referencia. La más común en las poblaciones deportistas, especialmente en mujeres, es la anemia per déficit de hierro (ferropénica). Esta situación, al afectar la concentración de Hb, afectaría el rendimiento al disminuir la capacidad de transporte de O2 en la sangre. Es importante sin embargo, no confundirla con una falsa anemia, ya que una de las adaptaciones que produce el entrenamiento de la resistencia es un aumento del volumen plasmático de la sangre, y esto induce algo que se llama una hemodilución de todos sus componentes, diagnosticando una posible anemia cuando en realidad no es así.
Referencias
Barbany, J.R., (2002). “Respiración y ejercicio físico ” en, Barbany, J.R. Fisiología del ejercicio físico y del entrenamiento. Editorial Paidotribo. Barcelona.
Calderón, FJ (2007). Fisiología Aplicada al Deporte. Editorial Tebar. 2ª edición. Madrid.
Bassett, DR. y Howley ET (2000). Limiting factors for máximum oxygen uptake and determinants of endurance perfomance. Med. Sci. Sports Exerc., Vol. 32, No. 1, pp. 70-84.
Mckee, T. y Mckee, JR. (2003). Bioquímica: La base molecular de la vida. 3ª edición. Editorial McGRAW-Hill. Madrid.
Nelson, D. y Cox, M. (2005). Principios de bioquímica Lehninger. 4ª edición. Editorial Omega.
Wilmore, JH. y Costill ,DL (2007). Fisiología del esfuerzo y del deporte. 6ª edición. Editorial Paidotribo. Badalona.

