
22 Jul Efectos de los Suplementos Nutricionales sobre las Adaptaciones al Entrenamiento de Resistencia
Jeffrey A. Rothschild 1, 2 y David J. Bishop 3,4
1 Sports Performance Research Institute Nueva Zelanda (SPRINZ), Universidad Tecnológica de Auckland, Auckland, Nueva Zelanda.
2 TriFit Performance Center, Santa Mónica, CA, EE. UU.
3 Instituto de Salud y Deporte, Universidad de Victoria, Melbourne, VIC, Australia.
4 Facultad de Ciencias Médicas y de la Salud, Edith Cowan Universidad, Joondalup, WA, Australia.
Resumen
El entrenamiento de resistencia produce una variedad de adaptaciones a nivel celular y sistémico que sirven para minimizar las interrupciones en la homeostasis corporal producida por el ejercicio. Estas adaptaciones se ven afectadas de manera diferencial por el volumen, la intensidad y el estado de entrenamiento así como por las opciones nutricionales que pueden mejorar o perjudicar la respuesta al entrenamiento. Se ha estudiado una gran cantidad de suplementos en el contexto de la mejora aguda del rendimiento, pero no se han estudiado con detalle los efectos de la administración continua de suplementos junto a los programas de entrenamiento de resistencia. Por ejemplo, suplementos como el bicarbonato de sodio y la beta-alanina pueden mejorar el rendimiento de resistencia y posiblemente las adaptaciones al entrenamiento durante el entrenamiento de resistencia porque afectarían la capacidad buffer y/o permitirían una mayor intensidad de entrenamiento, mientras que los antioxidantes como la vitamina C y la vitamina E podrían afectar las adaptaciones al entrenamiento al disminuir la señalización celular, pero tendrían un efecto menor sobre las variables asociadas al rendimiento. Además, existen datos limitados que sugieren que el nitrato dietario (en forma de jugo de remolacha), la creatina y posiblemente la cafeína, podrían potencialmente mejorar aún más la adaptación al entrenamiento de resistencia. Por lo tanto, el objetivo de esta revisión es examinar el impacto de los suplementos dietéticos en las adaptaciones metabólicas y fisiológicas al entrenamiento de resistencia.
Puntos clave
Muchos suplementos han sido estudiados en el contexto de la mejora aguda del rendimiento, pero los efectos de la suplementación continuada junto con los programas de entrenamiento de la resistencia no han sido descriptos con detalle.
Suplementos tales como bicarbonato de sodio, beta-alanina, nitratos, antioxidantes, cafeína y creatina en la dieta tendrían el potencial de modificar la respuesta adaptativa al entrenamiento de resistencia (ya sea de manera positiva o negativa) porque afectarían el equilibrio ácido-base, el estado redox, la señalización de la respuesta antioxidante o la carga acumulada de entrenamiento lo que finalmente afectaría las respuestas de señalización celular frente al entrenamiento.
Introducción
El entrenamiento de resistencia (sesiones repetidas de ejercicio continuo o ejercicio intermitente realizadas con el objetivo de mejorar el rendimiento de resistencia) produce adaptaciones metabólicas y morfológicas a nivel celular y sistémico, que permiten realizar ejercicios de intensidad submáxima con una perturbación homeostática pequeña [1]. Estas adaptaciones incluyen aumentos en el consumo de oxígeno máximo (VO2máx), en la actividad enzimática mitocondrial y en el contenido de proteínas en las mitocondrias, lo que provoca un cambio hacia una mayor dependencia de las grasas como fuente de combustible, un menor flujo glucolítico, una disminución en la acumulación de lactato a una tasa de trabajo dada y un control más estricto del equilibrio ácido-base [1- 3].
Las adaptaciones inducidas por el entrenamiento son la consecuencia de estímulos repetidos de sesiones de ejercicio individuales [3], y de la acumulación en el tiempo de cambios transitorios en la expresión génica inducidos por el ejercicio [4]. La manipulación de la intensidad y de la duración del entrenamiento son las principales variables que afectan la respuesta al ejercicio [5]. Sin embargo, la ingesta dietética también puede afectar las adaptaciones al entrenamiento a través de un aumento en el estímulo de ejercicio y/o a través de la potenciación o atenuación de las respuestas celulares frente a las perturbaciones inducidas por el ejercicio (Figura 1) [6].
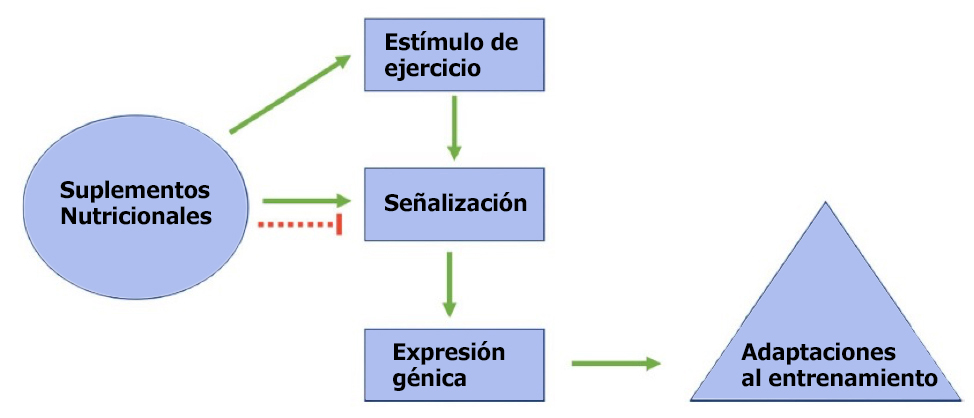
Figura 1. Impacto potencial de los suplementos sobre las adaptaciones al entrenamiento de resistencia. Las líneas solidas verdes representan aumentos mientras que las líneas discontinuas rojas representan inhibición.
Los atletas de élite utilizan mas suplementos dietéticos que los atletas que no son de élite, con una prevalencia similar entre hombres y mujeres [7]. Aunque las motivaciones para usar estos suplementos a menudo no tienen el objetivo de mejorar las adaptaciones al entrenamiento, el consumo de suplementos dietéticos representa un enfoque poco investigado y poco apreciado para modificar la respuesta adaptativa al entrenamiento de resistencia.
Los efectos sobre el rendimiento de los suplementos que consumen frecuentemente los atletas de resistencia, entre los que se incluyen el bicarbonato de sodio, la β-alanina y los nitratos dietéticos han sido estudiados [ 8-13]. Sin embargo, estos suplementos generalmente se consideran solo en el contexto de cambios agudos en el rendimiento y se dispone de poca información sobre cómo influyen en las adaptaciones al entrenamiento. Estos suplementos tienen el potencial de modificar la respuesta adaptativa al entrenamiento de resistencia (ya sea positiva o negativamente) por que afectan el equilibrio ácido-base, el estado redox, las vías de señalización de las especies reactivas del oxígeno (ROS), o la carga de entrenamiento acumulada, afectando así las respuestas de señalización celular al entrenamiento (Figura 2). Algunas discusiones sobre los efectos de los suplementos en las adaptaciones al entrenamiento han sido publicadas previamente [14-16], pero las mismas se centraron en un subconjunto estrecho de suplementos y no incluyeron estudios sobre creatina o cafeína, ni tampoco tuvieron en cuenta las investigaciones publicadas en los últimos 5 años. Por lo tanto, es necesario realizar una descripción actualizada de la literatura actual. El objetivo de esta revisión es examinar el impacto de los suplementos dietarios mas comunes sobre las adaptaciones metabólicas y fisiológicas al entrenamiento de resistencia
Agentes de Amortiguación (Buffers)
Los suplementos que actúan sobre la capacidad buffer (tampones) y la regulación del pH pueden afectar la respuesta al entrenamiento porque permiten que un atleta entrene más duro (aumentando el estímulo del ejercicio) y/o porque afectan las moléculas de señalización importantes, como las vías de la proteína quinasa activada por 5 ‘AMP (AMPK), la proteína quinasa activada por mitógeno p38 (MAPK) y la calmodulina quinasa dependiente de Ca2+ (CaMK), que se ven afectadas por el pH [17- 19].
Por ejemplo, se observó que un pH ácido disminuyó el contenido de proteínas AMPK fosforiladas en miotubos L6 diferenciados [19], fibroblastos cultivados [20] y cardiomiocitos de rata [21], mientras que un pH alcalino aumentó el contenido de proteínas AMPK fosforiladas en cardiomiocitos de rata [21]. En humanos, la inducción de acidosis con cloruro de amonio antes de una sesión de ejercicios intervalados redujo los aumentos posteriores al ejercicio en la proteína 1α coactivadora del receptor activado por el proliferador de peroxisomas (PGC-1α), en la citrato sintasa (CS), citocromo c (CYT-C) y GLUT4ARNm en comparación con un placebo [22] (Figura 3). Las concentraciones de lactato sanguíneo también disminuyen en condiciones de acidosis, probablemente debido a la atenuación de la actividad glucolítica [23]. Esto podría impactar negativamente en las adaptaciones al entrenamiento porque la señalización de lactato puede influir en la biogénesis mitocondrial [24] y en la respuesta adaptativa crónica al entrenamiento [25]. Un aumento en el pH de la sangre puede aumentar la tasa de degradación del glucógeno muscular junto con niveles crecientes de lactato en sangre y aumentar la salida de H+ hacia afuera en los músculos que se están contrayendo [26 ,27]. El aumento del pH de la sangre por consumo de bicarbonato de sodio antes de una sesión de ejercicios de alta intensidad aumentó la expresión del PGC-1α mRNA en mayor grado a lo que se observó en el placebo [27]. Aunque respuestas agudas al entrenamiento no siempre equivalen a adaptaciones a largo plazo [28], existe evidencia que sugiere que los suplementos que alterar el pH pueden afectar las adaptaciones al entrenamiento.
Bicarbonato de sodio
El bicarbonato de sodio generalmente se consume en una dosis de 0,2–0,4 g/kg de peso corporal, dividido en 1–3 porciones [16], aunque también se han utilizado protocolos de carga seriados durante varios días [29]. Esta dosis debe ser suficiente para elevar la concentración de bicarbonato en la sangre en 5–6 mmol/L y permite pequeños cambios en el pH de la sangre durante los ejercicios sub máximos, aunque se ha observado una gran variabilidad interindividual en la respuesta a la suplementación [30-32]. El consumo de bicarbonato de sodio antes de cada sesión de entrenamiento interválico de ciclismo (24 sesiones durante 8 semanas) en mujeres activas recreacionalmente produjo mayores mejoras en el umbral del lactato (26 frente a 15%, d=0,5) y en el tiempo hasta el agotamiento (164 vs. 123%, d=1,9) en comparación con un placebo, aunque el volumen y la intensidad del entrenamiento fueron similares entre los grupos (Tabla 1) [33]. Varones recreacionalmente activos realizaron seis semanas de entrenamiento intervalado de alta intensidad. (HIIT) (18 sesiones) donde consumieron bicarbonato de sodio o un placebo antes de cada sesión de entrenamiento y experimentaron una mayor mejora en la potencia máxima relativa (20,8 vs. 10,3%, d=2,1) pero no presentaron diferencias en la potencia media relativa alcanzada durante un test de Wingate [34] y presentaron mejoras similares en el tiempo hasta el agotamiento, la potencia máxima y la potencia en el umbral de lactato, aunque solo el grupo que consumió bicarbonato presentó un incremento significativo en la actividad de CS (22,3 vs. 12,6%) [35]. Por otra parte, 4 semanas de suplementación con bicarbonato de sodio en remeros varones altamente entrenados no produjeron beneficios significativos en el rendimiento en comparación a lo que se observó en los remeros que consumieron el placebo [36]. A pesar de que se observaron tendencias favorables en la potencia, la potencia máxima y la potencia en el umbral de lactato en 2000m es posible que la realización de solo ocho sesiones durante el período de estudio de 4 semanas y/ el pequeño tamaño de la muestra (n = 6 por grupo) no permitieran detectar cambios significativos.
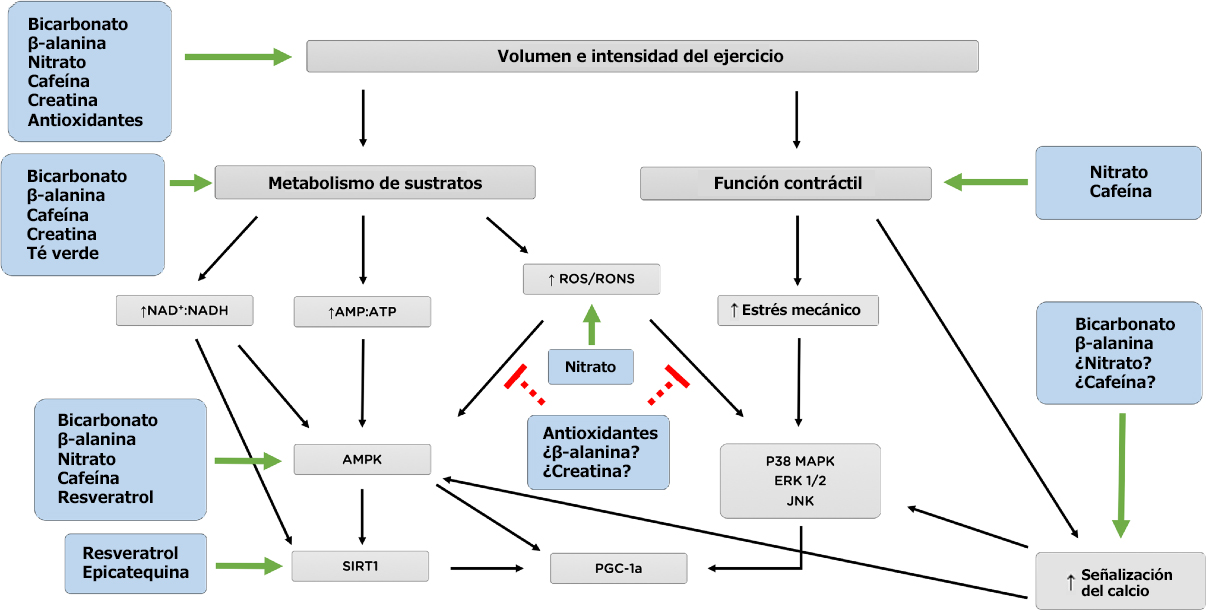
Figura 2. Esquema de las áreas donde los suplementos dietéticos pueden actuar para modificar las respuestas adaptativas al entrenamiento de resistencia. Línea continua verde: Estimulación (aumento), Línea discontinua roja: Inhibición (disminución). AMP= Adenosina monofosfato, AMPK 5 ‘ = Proteína quinasa activada por AMP, ERK1/2= Quinasa 1 y 2 regulada por señales extracelulares, NADH= Nicotinamida adenina dinucleótido, p38 MAPK= p38 proteína quinasa activada por mitógeno, PGC-1α =Proteína 1α coactivadora del receptor activado por el proliferador de peroxisomas, RONS= Especies reactivas de oxígeno y nitrógeno, SIRT1=Sirtuina 1; Signo de interrogación= Mecanismo posible
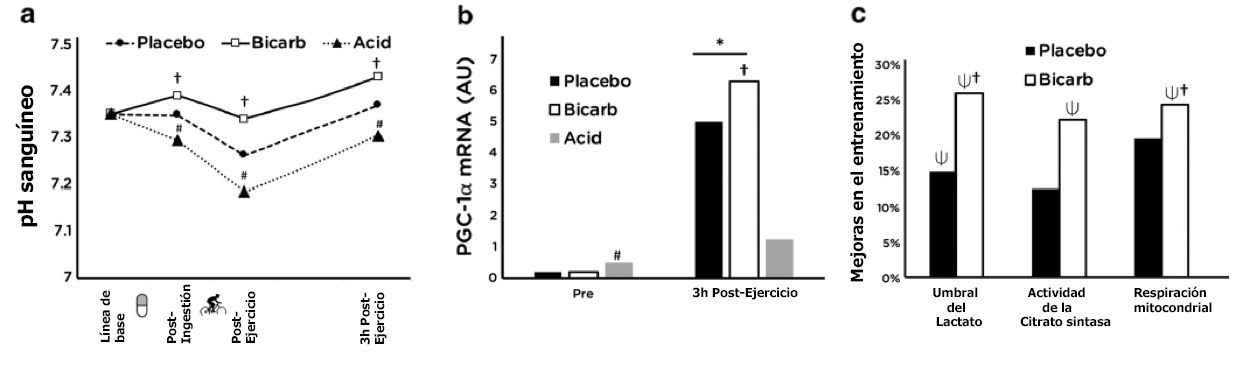
Figura 3. a) Respuestas del pH de la sangre al entrenamiento intervalado de alta intensidad luego del consumo de bicarbonato de sodio (Bicarb), cloruro de amonio (ácido), o un placebo, b) efecto del pH y del entrenamiento en PGC-1α, y c) Respuesta al entrenamiento. Un pH alcalino puede mejorar, mientras que un pH más ácido puede deteriorar, la respuesta aguda de ARNm de PGC-1α y las adaptaciones al entrenamiento intervalado de alta intensidad a largo plazo. PGC-1α= Proteína 1α coactivadora del receptor activado por el proliferador de peroxisomas. *Efecto principal del tiempo al comparar con los valores obtenidos pre-ingestión (P <0.01); †= presenta diferencias significativas con respecto al placebo en el momento señalado (P <0.01); # = se observaron diferencias significativas entre el grupo que consumió el placebo y el que consumió bicarbonato en el momento señalado (p <0,05); ⍦= se observaron diferencias significativas con respecto al valor obtenido pre-entrenamiento (p <0.05). Adaptado de [22, 27, 33, 35, 37].
| Participantes | Estado de entrenamiento | Duración | Dosificación del suplemento | Tipo de entrenamiento | Cantidad total de sesiones de entrenamiento | Rendimiento
( en comparación con un placebo) |
Adaptaciones (en comparación con el placebo | |
| Bicarbonato de Sodio | ||||||||
| Edge et al. (33). | 16 f | Activos Recreacionalmente | 8 semanas | 0,4 mg/kg peso corporal | HIIT 3/sem; 6-12×2 min intervalos de ciclismo a 140-170% de LT, 1 min RBI | 24 | Umbral del lactato (LT);: +26 vs 15% (d=0,5, [95% CI-0,5, 1,5])
Tiempo hasta el agotamiento: +164 vs123% (d=1,9, [95% CI-0,7, 3,1]) Ninguna diferencia en VO2max |
|
| Driller et al. [36] | 12 m | Bien entrenados | 4 semanas | 0,3 g/kg peso corporal | HIIT 2 ×/sem; intervalos de remo 8×2,5 min a 90% de PPO, 3 min RBI | 8 | Ninguna diferencia en rendimiento ni en LT | |
| Hawke et al. [35] | 19 m | Activos recreacionamlmente | 6 semanas | 0,4 g/kg peso corporal | HIIT 3 ×/sem; intervalos de ciclismo 8–12×2min a 85–110% VO2max, 1 min RBI | 18 | Ninguna diferencia en rendimiento ni en LT | Actividad de CS +22,3 vs 12,6% |
| Wang et al. [34]
|
20 m | Activos recreacionalmente | 6 semanas | 0,2 g/kg peso corporal | HIIT 3 ×/sem; 4 series de 20–30 s de ciclismo a 100% PPO, 30–40 s a 70% PPO, 1 min RBS | 18 | Mayor aumento en la potencia máxima de Wingate (20,8 vs. 10,3 % d=2,1 95% CI 1,0, 3,2])
Ninguna diferencia en la potencia media relativa de Wingate |
Mayor concentración de lactato máximo solo en el grupo que consumió bicarbonato |
| Bishop et al. [37] | 21 m ratas | N/A | 5 semanas | 0,05 g/kg peso corporal | HIIT 5×/sem; 7–12×2min intervalos en cinta rodante, 1 min RBI | 25 | Tiempo hasta el agotamiento: 12 veces vs. 8 veces mas largo que el grupo control (d=11,1, [95% CI-6,8, 15,3])
|
Mayores mejoras en la masa y en la masa y en la respiración mitocondrial (d=1,8, [95% CI-0,6, 3,1])
|
| Beta-alanina | ||||||||
| Smith et al. [57] | 46 m | Activos recreacionalmente | 6 semanas | 3 semanas 6 g/día y luego 3 semanas 3 g/día. | HIIT 3x/sem; intervalos de ciclismo 5-6x 2 min a 90-115% PPO, 1 min RBI | 18 | Ninguna diferencia en VO2max. Tiempo hasta el agotamiento en PPO de 110%: +18,7 vs 15,1% (d=0,3 [95% CI -0,4, 0,9]) | |
| Walter et al. [54] | 44 f | Activos recreacionalmente | 6 semanas | 3 semanas 6 g/día y luego 3 semanas 3 g/día. | HIIT 3x/sem; 5-6x intervalos de ciclismo de 2 min a 90-115% PPO, 1 min RBI | 18 | Ninguna diferencia en VO2max, ni en la potencia en el umbral ventilatorio. | |
| Bellinger et al. [61] | 14 m | Bien entrenados | 4 semanas | 65 mg/kg peso corporal/día | HIIT 2x/sem; 8 x 2,5 min intervalos de ciclismo a 90% VO2max HR | 8 | Sin diferencias en la potencia en pruebas contrarreloj de 4 min. | |
| Howe et al. [59] | 16 m | Bien entrenados | 4 semanas | 4,5 g/día | HIIT 2x/sem; 8 x 2,5 min a 90% PPO, 3 min RBI | 8 | Ausencia de diferencias en la potencia de contrarreloj de 4 min, tendencia hacia un mayor trabajo total realizado (p=0,09) | |
| Cochran et al. [55] | 24 m | Activos recreacionalmente | 6 semanas | 4 semanas de carga con 3,2 g/día, seguidas por 6 semanas de 3,2 g/día con entrenamiento supervisado | SIT 3x/sem; 4-6 Test de Wingate, 4 min RBI | 18 | Ausencia de diferencia en VO2max, capacidad de esprint repetido ni en el rendimiento de pruebas contrarreloj | Ausencia de diferencia en las actividades máximas de citocromo c oxidasa y de β-HAD |
| Bellinger y Minahan [53] | 14 m | Bien entrenados | 5 semanas | 4 semanas de carga con 6,4 g/d, luego con 5 semanas de 1,2 g/d con entrenamiento supervisado | SIT 2x/sem; esprints de ciclismo 4-6x 1 km (aprox. 1,3 min), 4 min RBI | 10 | Ninguna diferencia en rendimiento en pruebas contrarreloj ni en VO2max.
Intensidad de entrenamiento: +9,9 vs. 4,9% (d= 0,3, [95% CI − 0.8, 1.3]) Tiempo hasta el agotamiento a 120% PPO: +14,9 vs. 9,0% (d = 0.5, [95% CI − 0.6, 1.58]) |
|
| Santana et al. [58] | 16 m | Activos recreacionalmente | 23 días | 5 g/d | Moderada intensidad 2x/sem (7-12 km), HIIT 1x/sem (6×500 m esprints, 2 min RBI) | 9 | Rendimiento en running de 10 km: -6,7 % vs. Sin cambio. | |
| Wang et al. [56] | 38 m | Activos recreacionalmente | 4 semanas | 6,4 g/d | HIIT 2x/sem; tres series de 5 x 10 s esprints máximos, 20 s RBI, 5 min RBS. | 8 | Ausencia de diferencia en VO2max o en PPO
Capacidad anaeróbica: 14% mayor que el placebo (d=0,8 [95% CI – 0,1, 1,8]) |
Tabla 1. Descripción general de los estudios que utilizaron agentes buffer durante entrenamiento de resistencia supervisado. Tamaño de efecto de los suplementos calculado con d de Cohen en aquellos datos que estuvieran disponibles (informado como tamaño de efecto, 95% CI): HIIT = entrenamiento intervalado de alta intensidad; SIT= entrenamiento intervalado de esprint; TTE= Tiempo hasta el agotamiento; PPO= producción de potencia máxima; RBI= descanso entre intervalos; RBS= descanso entre series.
En un estudio realizado con ratas que realizaron HIIT en una cinta rodante cinco veces por semana durante 5 semanas se observó un tiempo hasta el agotamiento 52% mayor (d=11,1), y mayores mejoras en la respiración mitocondrial estimulada por ADP (d=1,8), cuando las ratas consumieron bicarbonato de sodio antes del ejercicio, en comparación con cuando ingirieron un placebo antes del ejercicio [37, 38]. Estos grupos también habían sido equiparados con respecto a la cantidad de trabajo total realizado durante cada sesión de entrenamiento, lo que apoya adicionalmente el potencial del bicarbonato para mejorar la adaptación al entrenamiento. Cambios en la actividad de CS y de la fosfo- fructoquinasa y en el contenido de proteína cotransportadora de bicarbonato de sodio, fueron similares al del grupo placebo [37, 38], a pesar de que los niveles de transportador de monocarboxilato 4 se incrementaron en mayor nivel después del entrenamiento con la suplementación con bicarbonato [38].
En general, es poco probable que el bicarbonato de sodio tenga un efecto en el VO2max (el cual se ve afectado en gran medida por las adaptaciones centrales [39 ]), pero puede afectar las adaptaciones periféricas que son influenciadas por el pH, tales como el umbral de lactato, la actividad de CS y la respiración mitocondrial, particularmente en personas sin entrenamiento (Figura 3). Los resultados contrastantes pueden deberse a diferencias en el estado físico, la cantidad y la intensidad de las sesiones de entrenamiento realizado, diferencias de sexo, genética y tamaño de muestra. Dos estudios que no observaron diferencias entre los grupos prescribieron el HIIT en forma de porcentaje de potencia máxima [35,36 ], mientras que un estudio que estableció la intensidad del entrenamiento como un porcentaje del umbral del lactato el umbral observó un mejor rendimiento [33].
Las investigaciones futuras deberían analizar las diferencias en el contenido de enzimas mitocondriales y en la respiración mitocondrial que se producen como resultado del consumo de bicarbonato de sodio antes de las sesiones de entrenamiento. Los estímulos de ejercicio deberían ser suficientes para alterar los niveles de lactato y/o el pH en comparación con el placebo, y deberían comparar intervalos similares tanto de trabajo como de tiempo (por ejemplo, intervalos de 4 minutos con esfuerzo máximo) para examinar los efectos de las diferencias en el pH vs diferencias en el trabajo total durante las sesiones de entrenamiento.
Beta-alanina
La beta-alanina es un suplemento cada vez más popular entre los atletas debido a su capacidad para retrasar la fatiga durante los ejercicios de alta intensidad. Lo hace aumentando el contenido de carnosina muscular de forma dependiente de la dosis [40 ], y se han observado mejoras en el rendimiento físico con dosis que varían de 3,2 a 6,4 g/día durante 4 a 24 semanas [9]. La β-alanina tiene el potencial para mejorar las adaptaciones al entrenamiento aumentando la capacidad de mantener el ejercicio a alta intensidad [41], lo que permite que los atletas toleren mejor un mayor volumen de entrenamiento con menos sentimientos subjetivos de fatiga [42]. Dado que la β-alanina se considera principalmente efectiva en un período que va de 1-10 minutos [ 9], los atletas de resistencia que realizan sesiones de entrenamiento intervalado dentro de esa duración pueden obtener beneficios de una mejor respuesta adaptativa al entrenamiento a través de la acumulación de una mayor carga de trabajo durante cada sesión. Esto podría deberse a una serie de factores interrelacionados, entre los que se incluye una mejora en la capacidad de amortiguación del pH [43], lo que permitiría una mayor dependencia del metabolismo aeróbico y, por lo tanto, una reducción de la acumulación de metabolitos glucolíticos en la misma intensidad de ejercicio [44], una disminución de los niveles de lactato en sangre durante la recuperación de ejercicio supramáximo [45], una reducción en el estrés oxidativo debido a los efectos antioxidantes de la carnosina que podrían permitir una mejor recuperación entre entrenamientos exigentes [46- 48], un mayor umbral para la fatiga neuromuscular [41] y/o una menor sensación de fatiga durante los períodos de entrenamiento pesado [42, 44]. También se ha sugerido que los aumentos en la sensibilidad al calcio [49], o en la recaptación de calcio [ 50 ], también puede desempeñar un papel en los efectos ergogénicos de la β-alanina porque ayudarían a frenar la disminución del rendimiento muscular durante los ejercicios fatigantes. Desde una perspectiva de señalización celular, la suplementación con β-alanina puede afectar la biogénesis mitocondrial a través del aumento de la recaptación de calcio [50] y por sus efectos corriente abajo sobre el AMPK, CaMK y sobre las quinasas reguladas por señales extracelulares 1 y 2 (ERK 1 y 2) [51], por un aumento de la expresión de receptores activados por el proliferador de peroxisomas (PPAR) β / δ [ 52], y /o por una mejor señalización de lactato [24, 53] (Figura 2).
La mayoría de los estudios han investigado los efectos de la β-alanina en el rendimiento físico, y existen relativamente pocos estudios que hayan considerado los efectos de la suplementación sobre las adaptaciones al entrenamiento (Tabla 1). De los estudios que observaron cambios en el VO2max después del entrenamiento de resistencia, ninguno observó una mayor mejora gracias a la suplementación en comparación con el placebo [53- 57]. Este hallazgo es similar a lo observado con el bicarbonato de sodio y es algo esperable debido a que los agentes de amortiguación tienen una mayor probabilidad de ejercer sus efectos en el músculo esquelético en lugar de a través de mecanismos centrales. Sin embargo, se observaron aumentos similares en las actividades máximas de la citocromo-c oxidasa y β-hidroxiacil-CoA deshidrogenasa (β-HAD) en varones activos pero no entrenados que consumieron β-alanina o un placebo durante 6 semanas de entrenamiento intervalado de esprint (SIT) (tres sesiones por semana) [55], lo que sugiere que la existencia de diferencias en las adaptaciones periféricas pueden no ser observadas cuando el trabajo total realizado es el mismo. Esto no coincide con algunos de los hallazgos observados con el bicarbonato de sodio [33, 34].
Se han observado mejoras de rendimiento luego de la suplementación con β-alanina en comparación con un placebo en el rendimiento de carreras contrarreloj de 10 km (~ 54 min) después de 3 semanas de entrenamiento de carrera [58 ], y en el tiempo hasta el agotamiento en ciclismo realizado a 120% de potencia máxima (~ 3.5 min) después de un programa SIT de 5 semanas [53] (Tabla 1). También se observó una tendencia a una mayor mejora en tiempo de ciclismo hasta el agotamiento al 110% de la potencia máxima (~ 23 min) después de 6 semanas de HIIT [57]. En contraste, 4–6 semanas de entrenamiento intervalado en participantes recreativamente activos que consumieron β-alanina o un placebo provocaron mejoras similares en el rendimiento de una prueba contrarreloj de 250 kJ (~ 20 min) [ 55], potencia promedio durante una prueba contrarreloj de 4 minutos [59], potencia en el umbral ventilatorio [54] y potencia crítica durante una prueba de ciclismo máximo de 3-min [56]. Teniendo en cuenta sus efectos establecidos en rendimiento de ejercicios de alta intensidad [9], es un desafío poder distinguir los efectos de la β-alanina sobre el rendimiento de sus efectos sobre las adaptaciones al entrenamiento. Sin embargo, tal como se observa en la Figura 4 la suplementación con SIT y β-alanina tendría beneficios tanto independientes como aditivos.
Uno de los mecanismos que han sido propuestos para explicar como la β-alanina mejora las adaptaciones al entrenamiento es una mayor intensidad de entrenamiento. Esto se observó en un estudio que observó mejoras [53], mientras que otro en estudio que observó aumentos favorables se observó una tendencia hacia una mayor intensidad del entrenamiento [57]. Por otra parte, se observó un aumento en los niveles de lactato sanguíneo durante los intervalos de esprint con suplementación, en comparación a lo que se observó con el placebo [53, 60]. Aunque las intensidades de entrenamiento no fueron informadas en otros dos estudios que observaron mejoras, utilizaron protocolos de entrenamiento intervalado que generaban niveles de esfuerzo máximo y no niveles de esfuerzo predeterminados [56, 58 ]. No se observaron diferencias en la intensidad del entrenamiento en estudios que no lograron producir aumentos adicionales con la β-alanina, ya sea con entrenamiento de esprint máximo (30 s) [ 55] o con esprints en intensidades de trabajo pre determinadas [54, 59 , 61]. Esto sugiere que las mayores adaptaciones al entrenamiento luego de la suplementación con β-alanina tienen una menor probabilidad de ser observadas si las intensidades de entrenamiento se sujetan intencionalmente o si las prescripciones de intervalo elegidas están fuera de rango de ejercicio de 1 a 10 minutos donde la β-alanina ejerce su influencia mas prominente [62 ]. Con regímenes de dosificación típicos de 3,2–6,4 g/día, se necesitan al menos 2 semanas de suplementación para elevar las concentraciones de carnosina muscular [40, 63], antes de que se produzcan los efectos beneficiosos sobre la intensidad del entrenamiento. Por lo tanto, la carga de carnosina muscular puede ser beneficiosa antes de emprender un estudio de entrenamiento físico.
Resumen
El uso de bicarbonato de sodio (que produce un cambio agudo en la capacidad buffer de la sangre) o el consumo de β-alanina (que provoca un cambio crónico en la capacidad buffer muscular) favorecerían potencialmente mayores adaptaciones al entrenamiento, aunque los datos no son del todo claros. Los resultados contrastantes pueden deberse a diferencias en el estado del entrenamiento, en la intensidad del entrenamiento o en el uso de prescripciones de intervalos que fijan intensidades de ejercicio y/o que pueden estar fuera de la duración óptima donde el suplemento es efectivo (p. ej. <60 s). Además, las respuestas al bicarbonato de sodio estarían sujetas a la variabilidad tanto intra-individual [31] como inter- individual [64], al menos en participantes no entrenados. Aunque los efectos sobre el rendimiento de la ingesta simultánea de bicarbonato de sodio y β-alanina no están claros [65], varios estudios han investigado los efectos de la suplementación combinada sobre adaptaciones de entrenamiento [66- 68 ]. Si bien generalmente se utiliza un período de carga de suplementación con β-alanina de 4 semanas cuando se estudia la co-ingestión, en todos los estudios menos en uno [61] las sesiones de entrenamiento de los participantes no fueron monitoreadas. Tal como se discutió previamente, las diferencias en la intensidad del entrenamiento serían necesarias para poder observar adaptaciones beneficiosas al entrenamiento con la suplementación con β-alanina.
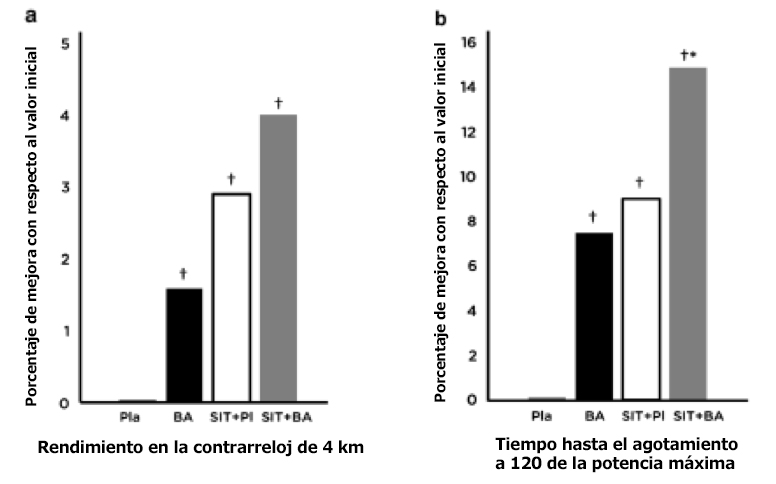
Figura 4. Aumento porcentual en el rendimiento de ciclistas entrenados en prueba contrarreloj de 4 km y b) tiempo hasta el agotamiento después de 4 semanas de suplementación con placebo y entrenamiento regular (Pla), 4 semanas de suplementación con beta-alanina y entrenamiento regular (BA), 5 semanas de entrenamiento intervalado de sprint y suplementación con placebo (SIT + Pla), 4 semanas fase de carga de beta-alanina seguidas de 5 semanas de entrenamiento intervalado de esprint con suplementación continua (SIT+BA). Los ciclistas que consumieron el suplemento de β-alanina y mantuvieron su entrenamiento normal (BA) presentaron un aumento de 1,6% en el rendimiento de la prueba contrarreloj de 4 km (~ 6 min) (d = 0,3) y una mejora del 7,5% en el tiempo hasta el agotamiento a 120% de la potencia máxima (d = 0,4), en comparación a la ausencia de cambios observada en el grupo placebo, mientras que 5 semanas de SIT con β-alanina provocaron una mayor mejora en el tiempo hasta el agotamiento (+14,9 vs. 9,0%, d=0,5) y una tendencia hacia una mayor mejora en el tiempo de rendimiento en la prueba contrarreloj en comparación con lo que se observó con el placebo, lo que sugiere que el SIT y la suplementación con β-alanina ejercen beneficios tanto independientes como aditivos. † Diferencias significativas con respecto al valor observado antes de la suplementación (pre-suplementación) (P <0,05), * diferencia significativa con respecto a SIT+Pla. Adaptado de [53, 60].
Las investigaciones que utilicen dosis que se sabe que aumentan el pH de la sangre o el contenido de carnosina muscular deben analizar los efectos a largo plazo de la suplementación con bicarbonato de sodio y β-alanina sobre la capacidad de entrenamiento para determinar si los atletas pueden aumentar su volumen de entrenamiento, lo que podría permitir mayores adaptaciones al entrenamiento y, a su vez, mejorar el rendimiento, así como también los efectos del estado del entrenamiento en las adaptaciones al entrenamiento. Particularmente respecto a la β-alanina, las prescripciones de intervalos deben evitar cargas de trabajo predeterminadas (p. ej., 4 min al 90% de potencia máxima), a favor de intervalos de distancia o de tiempo (p. ej., esfuerzos máximos de 1 km o 4 minutos). En aquellos casos en que sea necesario establecer cargas de trabajo, el uso de un porcentaje de umbral de lactato puede ser preferible frente al porcentaje de VO2max. Además del trabajo completado durante cada sesión, la medición de las concentraciones de lacto sanguíneo pueden ser útiles para determinar si los cambios en los niveles de lactato, en comparación con el placebo, pueden ser predictivos de una mayor respuesta al entrenamiento (Tabla 2).
Nitrato dietético
El nitrato dietético (NO3-), comúnmente suplementado y estudiado en forma de jugo de remolacha, tiene el potencial de aumentar las adaptaciones al entrenamiento de resistencia debido a su habilidad para aumentar los niveles plasmáticos de nitrito (NO2–) y óxido nítrico (NO) [69]. Puede aumentar la intensidad del entrenamiento [70] (y por lo tanto la cantidad total de trabajo completado en un entrenamiento) porque aumenta la eficiencia mitocondrial [71], reduce el costo de oxígeno de la contracción muscular [72 ] y porque aumenta la fuerza contráctil en músculos de contracción rápida [73]. También se han observado aumentos en la biogénesis mitocondrial (a través de la estimulación de la guanilato ciclasa con NO que conduce a activación de PGC-1α) [74 ], y cambios en el tipo de fibra muscular hacia un fenotipo más oxidativo cuando se combina con SIT (a través del papel del óxido nítrico en la calcineurina-NFAT [factor nuclear de señalización de células T activadas] [75 -77], lo que posiblemente se relacione con aumentos en peróxido de hidrógeno mitocondrial [78]. Sin embargo, al reducir el costo de oxígeno de la contracción muscular, lo que a su vez reduce el estrés metabólico dentro del músculo, también es posible que la suplementación con nitrato pueda afectar la adaptación al entrenamiento a través de la disminución de la activación de las vías de señalización celular (por ejemplo, AMPK, CaMK y PGC-1α) [79].
La mayoría de los estudios que observaron que la suplementación ejerce efectos beneficiosos en el rendimiento de resistencia han utilizado dosis de 6–8 mmol NO3– tomadas en forma de dosis única 2–3 h antes de ejercicio o con un período de carga de 5 a 8 días [10], pero los atletas de elite podrían necesitar dosis más altas (p. ej., 8–12 mmol) [80]. Los niveles plasmáticos de NO2–, que se usan como marcadores de la disponibilidad de NO [81 ], se incrementan de forma dependiente de la dosis pero los beneficios pueden alcanzar una meseta (plateau) entre 8 y 16 mmol NO 3– [82 ]. No se observaron efectos del jugo de remolacha después de 6 semanas de ciclismo HIIT cuando se ingirieron aprox. 5 mmol de NO3– por día [83], pero estudios de entrenamiento que implementaron una con suplementación de 8–12,8 mmol de NO3– por día observaron beneficios [75 , 84- 86].
Siete estudios implementaron suplementación con nitrato dietario mientras realizaban entrenamiento supervisado de resistencia durante al menos 3 semanas [75, 77, 83 – 87 ] (Tabla 3). Cuatro semanas de SIT combinado con suplementos de jugo de remolacha provocaron mejoras inducidas por el entrenamiento en el VO2max de 7,7 a 10,7% [75, 85], que fueron mayores que con SIT solo (+ 5,6%) o después de SIT con suplementación con nitrato de potasio (KNO3) (+ 4,2%) [85 ]. El tiempo hasta el agotamiento durante el ciclismo de alta intensidad (potencia en el umbral de intercambio gaseoso más el 85% de la diferencia entre esa tasa de trabajo y VO2max) también presentó mejora superior con SIT + jugo de remolacha (+71%) en comparación con SIT solo (+ 47%) y SIT +KNO3 (+ 42%) [85]. Se han observado mayores reducciones en la presión sanguínea con SIT + jugo de remolacha en comparación con SIT + KNO3, una disparidad que también ha sido observada entre el consumo de jugo de remolacha y NaNO3 [88] y esto podría estar relacionado con la presencia de otros compuestos bioactivos encontrados en el jugo de remolacha [89]. Aunque es algo especulativo, la mayor disminución del NO2– plasmático que se observa durante el ejercicio con SIT + jugo de remolacha en comparación con SIT + KNO3 podría estar sugiriendo que existiría una mayor síntesis de NO durante el ejercicio, y coincide con las correlaciones observadas entre la disminución de NO2– en el plasma y con las mejoras en rendimiento físico [90]. Dos de los estudios de entrenamiento utilizaron NaNO3 como fuente de nitrato (6,5 y 11 mmol por día), y ninguno observó mejoras adicionales en el rendimiento [77, 87]. Las futuras investigaciones deberían analizar los efectos de la suplementación con diferentes fuentes de nitrato en la dieta sobre las adaptaciones al entrenamiento de resistencia.
Al igual que los buffers, el nitrato dietario actúa mayormente sobre el metabolismo periférico y no es esperable que la ingesta a corto plazo tenga una influencia apreciable en el VO2max. Una explicación para la mejora observada en el VO2max puede estar relacionada con cambios en el tipo de fibra muscular. El porcentaje de fibras de contracción lenta está directamente relacionado con el VO2max y el rendimiento de resistencia [91, 92], y los dos estudios que observaron un aumento adicional en VO2max luego de la suplementación también observaron cambios en la composición del tipo de fibras [75, 85]. Se observó una disminución de la proporción de fibras musculares de tipo IIx en el vasto lateral en el grupo que consumió nitrato en comparación con el grupo que consumió el placebo [75], y se observó un mayor aumento en la proporción de fibras tipo IIa después de SIT solo (+ 20%) y SIT + jugo de remolacha (+ 14%), en comparación con SIT + KNO3 (disminución no significativa) [85]. No está claro si estas diferencias sugieren que SIT + KNO3 no es tan efectivo como SIT solo, o si esto pone en evidencia la variabilidad y/o confiabilidad de las mediciones del tipo de fibra, que según los informes tienen coeficientes de variaciones entre biopsias de 21,5, 15,4 y 42,0% para las fibras de tipo I, IIa y IIx, respectivamente [93]. Cinco semanas de SIT en condiciones de hipoxia con suplementos de NaNO3 también provocaron aumentos en la cantidad relativa de fibras de tipo IIa, que no se observó con suplementos de placebo en normoxia o hipoxia, aunque se observaron mejoras similares entre los grupos en el VO2máx, el umbral de lactato y en la actividad de la CS [77]. Esto coincide con lo observado en una investigación in vitro que demostró que el nitrato aumentó la expresión del gen PGC-1α y produjo un cambio hacia las fibras musculares tipo I y IIa [94].
Dos estudios analizaron los efectos del nitrato dietario en las adaptaciones al entrenamiento 1–7 días después de haber terminado la suplementación [87, 95]. Un estudio se realizó con sujetos activos recreacionales que mantuvieron sus hábitos de ejercicio típicos y luego de veintiocho días de suplementación con NO3– realizaron pruebas de ejercicios después de 1 día de consumo de placebo o de nitrato continuo para estudiar el efecto de una dosis crónica+aguda versus el efecto de dosis crónica sola [95]. Se observó una reducción en el costo de oxígeno de ciclismo sub máximo incluso hasta 24 h después de consumir la dosis final de NO3– , que era similar a lo observado después de 28 días de suplementación seguidos de una dosis aguda de NO3– antes de la prueba [95]. Existen varias potenciales explicaciones para esta observación, entre las que se incluyen mejoras duraderas en la eficiencia mitocondrial [71] o del músculo contráctil [72] producidas por la suplementación crónica, o que a pesar de que las concentraciones plasmáticas de nitrito regresan a los valores de la línea de base después de 24 h, la disponibilidad de NO se mantuvo elevada como resultado del almacenamiento de NO2– y NO3– en el musculo esquelético [96]. En otro estudio se analizó el efecto de 3 semanas de HIIT de alto volumen en participantes activos recreacionales que consumieron ~ 11 mmol NaNO3– por día o un placebo, y realizaron una serie de pruebas de ejercicio 2–7 días después del último día de suplementación [87]. El consumo total de oxígeno disminuyó en un 5% en el grupo que consumió el suplemento pero no en el grupo placebo durante una prueba de agotamiento al 80% Wmax que fue realizada 4–5 días después de haber finalizado la suplementación, pero no se observaron diferencias entre grupos en las mejoras en el tiempo mismo o en VO2max [87]. En general, los datos limitados sugieren que los efectos beneficiosos de la suplementación con NO3– en el consumo de oxígeno durante el ejercicio submáximo pueden continuar observándose hasta por 5 días, pero los mecanismos y la evolución en el tiempo exacta del período de lavado (washout) deben ser establecidos con detalle.
Resumen
Existe evidencia limitada que sugiere que existirían pequeños efectos favorables de la suplementación con nitrato sobre el entrenamiento de resistencia, que posiblemente estén relacionados con cambios en el tipo de fibra muscular. El jugo de remolacha puede ser más efectivo que las sales de nitrato, aunque la eficacia de la suplementación puede verse afectada por la variabilidad interindividual [97] y por las condiciones ambientales [98]. Todos los estudios hasta la fecha han utilizado protocolos de entrenamiento de alta intensidad, ya que el nitrato dietario es particularmente efectivo para aumentar las respuestas fisiológicas en fibras de tipo II [99]. Se necesitan estudios que utilicen otras formas de entrenamiento de resistencia para diferenciar los beneficios ergogénicos agudos de los efectos crónicos del nitrato dietario sobre las adaptaciones al entrenamiento. Se necesitan mas investigaciones para determinar el rol de oxido nítrico en la biogénesis mitocondrial [74], así como también para investigar las diferencias en las respuestas de remodelación del músculo esquelético particularmente entre sujetos no entrenados y entrenados en resistencia (Tabla 2).
| Mecanismos de acción | Ingesta | Tipo de entrenamiento | Variables de medición | |
| Bicarbonato de sodio | Mayor intensidad de entrenamiento
Aumento en el pH→Mayor adaptación mitocondrial. |
0,2-0,4 g/kg de peso corporal son suficientes para aumentar el [HCO3−] en 5-6 mmol | Entrenamiento intervalado suficiente para elevar los niveles de lactato y/o el pH en comparación con el placebo. | Umbral del lactato
Masa y respiración mitocondrial. Tiempo hasta el agotamiento en esfuerzos máximos o cercanos al máximo Rendimiento en prueba contrarreloj |
| β alanina | Mayor intensidad de entrenamiento
Aumento en el pH→ Mayor adaptación mitocondrial Mayor sensibilidad al Ca Disminución en la peroxidación de lípidos |
2-4 semanas de fase de carga de 4-6 g/día y luego 3-6 g/día | Intervalos de 1-4 min con esfuerzos máximos en lugar de tasas de trabajo pre determinadas, suficientes para elevar el lactato sanguíneo en comparación con un grupo placebo | Tests de ejercicios con finales abiertos (ej. Tiempo hasta el agotamiento) en lugar de tests con puntos finales fijos (ej. Pruebas contrarreloj)
Intensidad de entrenamiento Estrés oxidativo |
| Nitrato dietario | Mayor intensidad de entrenamiento | 8-13 mmol/día aportados por jugo de remolacha | Intervalos de 15 s a 4 min utilizando esfuerzos máximos en lugar de tasas de trabajo pre determinadas, resistencia en estado estable | Masa y respiración mitocondrial
Cambios en el tipo de fibra muscular Intensidad de entrenamiento VO2max |
| Antioxidantes | El menor estrés oxidativo permite un mejor entrenamiento y una mejor recuperación
Estimulan o inhiben las vías de señalización vinculadas al estrés Estimulan la biogénesis mitocondrial |
Para poder plantear recomendaciones es necesario que se realicen mas investigaciones, particularmente respecto al momento de consumo en relación al ejercicio. | Para poder plantear recomendaciones es necesario que se realicen mas investigaciones. | Adaptaciones mitocondriales
Cambios en el rendimiento Intensidad de entrenamiento. |
| Cafeina | Aumento en la intensidad del entrenamiento a través de la menor percepción de esfuerzo
Mejora en la sensibilidad al Ca Mejor señalización AMPK |
2-6 mg/kg | Intervalos de 0,5-4min utilizando esfuerzos máximos en lugar de tasas de trabajo pre-establecidas | Masa y respiración mitocondrial
Intensidad del entrenamiento |
| Creatina | Mayor intensidad de entrenamiento
Mayor producción de energía Disminución en la peroxidación de lípidos |
10 g/día durante 10 días, luego 10 g/día durante los días de entrenamiento solamente. Es necesario realizar investigaciones adicionales. | Intervalos de 15 s a 4 min utilizando esfuerzos máximos en lugar de tasas de trabajo pre-establecidas. | Respiración mitocondrial
Intensidad de entrenamiento Rendimiento en pruebas contrarreloj. |
Tabla 2. Mecanismos propuestos y recomendaciones para estudiar las adaptaciones al entrenamiento de resistencia.
| Participantes | Nivel de entrenamiento | Duración | Dosis de suplementación | Tipo de entrenamiento | Cantidad total de sesiones de entrenamiento | Rendimiento (comparación con un grupo que consumió un placebo) | Adaptaciones (comparación con un grupo que consumió un placebo) | |
| Puype et al. [83] | 22 m | Moderadamente entrenados | 6 semanas | Aprox. 5 mmol/día (0,07 mmol NO3–/kg de peso corporal) | 30 min a 4-6 mmol/L de lactato sanguíneo, 5x/semana en hipoxia normobárica | 30 | Ausencia de diferencias en VO2max, LT ni en el rendimiento de prueba contrarreloj | |
| De Smet et al. [77] | 27 m | Activos recreacionales | 5 semanas | 6,5 mmol NaNO3 | SIT 3x/sem en hipoxia normobárica; 4-6 Test de Wingate, 4,5 min RBI | 15 | Ausencia de diferencias en VO2max, LT ni en el rendimiento de prueba contrarreloj | Mayor porcentaje de fibras de tipo IIa. No se observaron diferencias en la actividad de CS |
| Muggeridge et al. [84] | 27 m | Activos recreacionales | 3 semanas | Aprox. 8 mmol de nitrato [0.06–0.15 mmol/kg
Peso corporal] |
SIT 3x/semana; 4-6x esprints máximos, 4 min RBI | 9 | Tasa de trabajo máxima durante ejercicio incremental:+8,7 vs 4,7% (d=0,3, [95% CI − 0.6, 1.2]). No se observaron diferencias en VO2max. | |
| Thompson et al. [75] | 18 m, 18f | Activos recreacionales | 4 semanas | 12,8 mmol NO3– por día (2 porciones de 6,4 mmol, AM/PM) | SIT 3-4x/semana; 4-5 test de Wingate, 4 min RBI | 14 | VO2max: +8,8 vs 2,0% (d=0,2 [95% CI − 0.6, 1.0])
Tasa de trabajo máxima durante ejercicio incremental: +7,7 vs 5,0% (d=0.1, [95% CI − 0.7, 0.9]) Ausencia de diferencia en el tiempo hasta el agotamiento a elevada intensidad. |
Menor proporción de fibras musculares de tipo IIx en el vastus lateralis |
| Thompson et al. [85] | 18 m, 12f | Activos recreacionales | 4 semanas | 12,8 mmol NO3– por día (2 porciones de 6,4 mmol, AM/PM) | SIT 3-4x/semana; 4-5 Test de Wingate, 4 min RBI | 14 | VO2max: + 10.7 vs.5.6%
(d=0.2, [95% CI – 0,7, 1.0]) Tiempo hasta el agotamiento: + 71 vs. 47% (d=0.4, [95% CI − 0,5, 1,3]) Ausencia de diferencias en la tasa de trabajo máxima durante ejercicio incremental. |
|
| Finkel et al. [87] | 17 m | Activos recreacionales | 3 semanas | Aprox. 11 mmol/día (0,14 mmol NaNO3/ kg peso corporal) | HIIT 3x/sem; 45 intervalos de 30 s a 10 semanas por debajo de Wmax, 30 s recuperación a 10 w | 9 | No se observaron diferencias en VO2max, Wmax, ni en el tiempo hasta el agotamiento a 80% Wmax.
Aumento en la potencia solo en el grupo placebo durante el primero de dos test de Wingate (6%; d=− 0,5, [95% CI -1,4, 0,5), mejoras similares en el segundo test. |
|
| Santana et al. [86] | 16 m | Activos recreacionales | 4 semanas | Aprox. 12 mmol/día (en forma de tres porciones) | Moderada intensidad 2x/sem (5-12 km)
HIIT 1x/sem (4-6 x 500 m esprints, 2 min RBI) 10 km de prueba contrarreloj semanales. |
12 | Tiempo de carrera de 10 km: -9.1 vs.−1.0%
(d=1,2, [95% CI –2,3,−0,2]) Ausencia de diferencias en el Test de Wingate de 60 s. |
Tabla 3. Generalidades del consumo del nitrato dietario durante entrenamiento de resistencia supervisado. Tamaño de efecto de los suplementos calculado con d de Cohen en aquellos datos que estuvieran disponibles (informado como tamaño de efecto, 95% CI): HIIT = entrenamiento intervalado de alta intensidad; SIT= entrenamiento intervalado de esprint; TTE= Tiempo hasta el agotamiento; PPO= producción de potencia máxima; RBI= descanso entre intervalos; RBS= descanso entre series; Wmax= Potencia aeróbica máxima.
Antioxidantes
Los radicales libres se producen durante el metabolismo aeróbico y desempeñan un papel tanto en la fatiga inducida por el ejercicio como en la respuesta adaptativa al mismo [100]. La fuerza contráctil muscular disminuye por niveles elevados de especies reactivas de oxígeno y nitrógeno (RONS), en gran parte debido a los cambios en la sensibilidad al calcio de las miofibrillas [101]. Al mismo tiempo, las RONS generadas durante el ejercicio actúan como moléculas de señalización para aumentar la producción de proteínas involucradas en la adaptación del músculo esquelético al ejercicio tales como la NO sintasa, superóxido dismutasa (SOD) y MAP quinasas p38, ERK1 y ERK2 (Figura 2) [102 ,103]. Por ejemplo, las RONS, a través de la activación de AMPK, pueden inducir la actividad del promotor PGC-1α y la expresión de ARNm [104]. Debido a la capacidad para reducir las RONS, los antioxidantes tienen el potencial de perjudicar las respuestas adaptativas frente a los factores de estrés inducidos por RONS y, por lo tanto, afectar negativamente las adaptaciones al entrenamiento favorables que se producirían normalmente [105], mientras que también tendrían el potencial para mejorar la recuperación y el rendimiento agudo [106-108]. Algunos antioxidantes, entre los que se incluyen los polifenoles, pueden ejercer sus efectos en áreas que van más allá de la señalización por RONS, tales como como una mayor movilización de ácidos grasos [109] o la activación de sirtuin 1 (SIRT1) (Figura 2 ) [110]. Para acceder a una discusión adicional de los efectos de la suplementación con antioxidantes en el rendimiento físico, el lector puede remitirse a revisiones recientes [14, 105, 111].
Vitaminas C y E
Las vitaminas C y E son vitaminas antioxidantes que protegen a las organelas celulares del daño oxidativo [112, 113]. No se han observado efectos en las variables asociadas al rendimiento físico en estudios realizados con humanos cuando se consumieron suplementos con vitaminas C y/o E durante el entrenamiento de resistencia controlado [114- 125] (Tabla 4 ). En sujetos saludables, las adaptaciones del músculo esquelético, tales como aumentos inducidos por el entrenamiento en la actividad de la CS o de la β-HAD, en los niveles de ARNm o de proteínas de la subunidad citocromo c oxidasa IV (COX-IV), proteínas de heat-shock 70, o cambios en la oxidación de sustratos, no han sido afectados por la suplementación después de 4 a 12 semanas de entrenamiento [120, 123-126]. En contraste, la suplementación con vitaminas C y E durante 4–11 semanas redujo los aumentos inducidos por el entrenamiento en COX-IV, PGC-1α, PGC-1β, PPARγ, SOD y en la proteína GPx en comparación con un placebo tanto en sujetos no entrenados como en sujetos previamente entrenados [122, 127]. Los estudios realizados en animales también han demostrado que 4–14 semanas de entrenamiento aeróbico junto con ingesta de antioxidante disminuyeron los aumentos inducidos por el entrenamiento en la actividad de la citocromo oxidasa y de CS, del factor de transcripción mitocondrial A (TFAM), CYT-C, GPx, glutatión reductasa, SOD, PGC-1α, NRF-1 y NRF-2 [ 118 ,128- 130], aunque otras investigaciones no observaron ningún efecto sobre los marcadores de la adaptación al entrenamiento tales como la capacidad respiratoria mitocondrial y contenido de proteínas CYT-C, COX-I, COX-IV, CS, NRF-1 o PGC-1α [130- 133].
La falta de consistencia entre los resultados, particularmente en las investigaciones realizadas en animales, podría estar relacionada a variaciones en la dosificación, en los protocolos de ejercicio y en los niveles basales de antioxidantes endógenos. La cantidad de antioxidantes proporcionada tiene una diferencia de más de diez veces [128, 134], el tipo de ejercicio incluyó carrera y natación y la duración de las sesiones de entrenamiento osciló entre 30 min y 6 h/día [132-134]. Además es necesario considerar potenciales redundancias en el proceso de adaptación. Por ejemplo, la contracción del músculo esquelético activa la AMPK aguas arriba a través de su quinasa Ca 2+/ o quinasa de calmodulina quinasa (CaMKK) [135] y los cambios en las proteínas que regulan el metabolismo de las grasas como FAT/CD36 están mediados en parte por la señalización inducida por contracciones de la vía ERK1/2 [136]. Por lo tanto, muchas de las adaptaciones comunes al entrenamiento de resistencia se pueden observar en ausencia de señalización RONS y pueden estar mínimamente influenciadas por la suplementación con antioxiantes.
También es necesario considerar que algunos efectos pueden perderse debido a las muestras de pequeño tamaño. Por ejemplo, los dos estudios realizados en humanos que observaron una disminución en las adaptaciones al entrenamiento luego de suplementación con antioxidantes también tenían el mayor tamaño muestral [122, 127]. De manera contraria, 8 semanas de entrenamiento de resistencia con o sin suplementación no tuvieron un efecto estadístico sobre los aumentos en VO2max, pero el grupo que consumió vitamina C (n=5) experimentó una mejora de 10,8% mientras que el grupo sin suplementación (n = 9) presentó una mejora de 22% (d = -1.0) [118].
Los efectos de la suplementación con vitamina C y E en los niveles de los marcadores de estrés oxidativo también han sido variables, y hay estudios que han informado reducciones [116], aumentos [ 119 , 137] o ningún impacto [123, 138]. Esto podría estar relacionado principalmente con problemas metodológicos que incluyen el uso de pruebas cuyo empleo ya no es recomendable, la corta semivida de los oxidantes que están siendo medidos y la falta de especificidad de medición, lo que dificulta tanto la realización como la interpretación de las investigaciones disponibles [139- 141]. Se necesita más investigación antes de poder arribar a una conclusión sobre el impacto que tienen las vitaminas C y E en los marcadores de estrés oxidativo durante el entrenamiento de resistencia.
Polifenoles
Los polifenoles son antioxidantes que se encuentran en las plantas y tienen la posibilidad de afectar las adaptaciones crónicas al entrenamiento de resistencia por varios mecanismos diferentes a los de las vitaminas C y E. En lugar de actuar como secuestrantes (scavengers), pueden estimular las vías de señalización celular relacionadas con el estrés y aumentar la expresión de genes que codifican proteínas tales como NRF2, y también estimular la vía SIRT1–AMPK – PGC1α en el músculo esquelético, que conduce a un aumento de la biogenesis mitocondrial (Figura 2) [142]. Quizás, paradójicamente para el atleta de resistencia, se cree que la activación de AMPK depende de la capacidad de los polifenoles, como la quercetina y el resveratrol, para unir e inhibir directamente el complejo mitocondrial F1F0- ATPasa/ATP sintasa (Complejo V), afectando negativamente la producción de ATP [143]. Varios estudios han investigado el efecto de los polifenoles en el rendimiento físico [142 ]; sin embargo, pocos estudios incluyeron programas de entrenamiento de resistencia supervisados (Tabla 4 ).
4.2.1 Resveratrol
El resveratrol es un polifenol que se encuentra en las uvas, el vino tinto y otras especies de plantas, y se sabe que activa SIRT1 [110], puede inducir un cambio en las fibras musculares hacia un fenotipo más oxidativo [144]. La suplementación con resveratrol durante 8 semanas de HIIT en varones sedentarios atenuó las mejoras inducidas por el ejercicio en VO2max y en la carbonilación de proteínas, pero no tuvo efecto sobre la actividad de PGC-1α ARNm, CYT-C, CS y β-HAD, ni en el tiempo hasta el agotamiento en pruebas de extensores de rodilla realizadas con una sola pierna, en comparación con lo que se observó en el placebo [145, 146 ]. En contraste, en un estudio con varones activos recreacionales que realizaban HIIT, 4 semanas de suplementación con resveratrol no produjeron diferencias en los aumentos inducidos por el entrenamiento en VO2máx , potencia aeróbica máxima, potencia de Wingate, actividad de succinato deshidrogenasa, ni en la distribución de tipo de fibra, en comparación con el placebo, aunque el grupo que consumió el resveratrol presentó aumentos menores en la expresión génica de PGC-1α, SIRT1 y SOD [147]. Esto coincide con lo observado en investigaciones realizadas in vitro que observaron que la exposición aguda a resveratrol inhibe la actividad de AMPK en las células del músculo esquelético humano [148]. Después de 12 semanas de entrenamiento en cinta rodante con suplementación con resveratrol, las ratas criadas para aumentar la capacidad de resistencia presentaron una mayor activación de la vía AMPK– SIRT1 – PGC-1α y VO2max [ 149 ], mientras que las ratas criadas para una baja capacidad aeróbica no presentaron diferencias en los niveles de VO2máx., AMPK o SIRT1 [150], lo que sugiere que la respuesta al resveratrol puede estar influenciada por el estado de entrenamiento. Los datos disponibles sobre el resveratrol son limitados pero sugieren que humanos y animales activos/entrenados pueden responder de manera diferente a aquellos que son sedentarios / no entrenados.
Extracto de té verde
Los extractos de té verde son un tipo de flavonoides polifenólicos que, más allá de su papel como antioxidantes, también pueden desempeñar un papel en la movilización y oxidación de los ácidos grasos [151] que parecen estar mediadas, al menos en parte, por la reducción de contenido de malonil-CoA en el músculo esquelético [152 ]. En varones sanos, el consumo de suplementos de extracto de té verde mientras realizaban entrenamiento de resistencia durante 10 semanas de intensidad moderada provocó una mayor oxidación de grasas durante ejercicios de ciclismo a 55% VO2max, pero no se observaron cambios en el grupo placebo [109] (Tabla 4). Varones desentrenados que realizaron una intervención de entrenamiento de 4 semanas y consumieron extracto de té verde o placebo experimentaron mejoras similares en VO2máx y en el tiempo hasta el agotamiento en carreras (08.01 a 09.07 km/h con pendiente de 18-20%), pero no se observaron diferencias entre grupos en el estado antioxidante [153 ]. Sin embargo, estas son tareas de rendimiento que no se beneficiarían de un aumento en las tasas de oxidación de grasas porque tienen una intensidad que dependería de oxidación de los carbohidratos [154]. Ratones que realizaron entrenamiento de resistencia durante 10 semanas y consumieron suplementos de extracto de té verde presentaron mejores tiempos hasta el agotamiento en carrera (~ 2.5 h) y natación (~ 40 min) en comparación con el grupo que solo realizó ejercicio, y además niveles más altos de β-oxidación muscular y FAT/CD36 mRNA [152, 155]. La escasez de datos de análisis del extracto de té verde en el contexto del entrenamiento de resistencia apoya el noción de que produce un aumento en la oxidación de grasas y mejora en el tiempo hasta el agotamiento durante los ejercicios en animales pero no en varones no entrenados; Por otra parte, se necesitan estudios que incluyan otras medidas de rendimiento (por ejemplo, pruebas contrarreloj), particularmente en intensidades y duraciones que puedan favorecer una mayor oxidación de las grasas.
Otros antioxidantes
Suplementación con (-)epicatequina, un componente del cacao que se sabe que activa la vía SIRT1 [156 ], anuló las adaptaciones al entrenamiento logradas durante 4 semanas de entrenamiento de ciclismo; se observaron aumentos en VO2max (+ 22,6%) y en la actividad de la succinato deshidrogenasa (+59,1%) en el grupo placebo pero no en el grupo que consumió el suplemento, y no se observaron diferencias entre los grupos en la potencia máxima ni en la actividad de la CS [ 157] (Tabla 4). En contraste, los ratones sometidos a entrenamiento en cinta rodante tuvieron mayor aumento en el tiempo hasta el agotamiento, en los niveles de CS y en los niveles de proteínas PGC-1β y TFAM luego de la suplementación con (-)-epicatequina en comparación al grupo que solo realizó ejercicios [158 ]. El consumo de allopurinol (un inhibidor de la xantina oxidasa) en ratas durante 6 semanas no ejerció ningún efecto sobre los aumentos inducidos por el entrenamiento en PGC-1α, TFAM, ni en la expresión de proteínas CYT-C, ni en la actividad de las enzima CS y β-HAD, a pesar de la atenuación de proteínas clave de señalización (p38 MAPK, ERK1/2 y TFAM) después de una sola sesión de ejercicio [103 ,159], lo que destaca la importancia de estudiar adaptaciones al entrenamiento de resistencia a largo plazo.
Resumen
Mejoras de rendimiento relacionadas con la resistencia después de programas de entrenamiento de 1 a 6 meses no se vieron afectados por suplementación con vitamina C y/o vitamina E, y es poco probable que se vean afectadas por otros antioxidantes, aunque hay menos datos disponibles. Menos claros son los efectos de las vitaminas C y E sobre los marcadores de adaptaciones de entrenamiento y estrés oxidativo. La falta de conexión entre una respuesta adaptativa afectada negativamente sin disminuciones de rendimiento medibles puede hacer que sean necesarios períodos de tiempo mayores antes de que las diferencias observables en el rendimiento puedan ser detectadas. Las diferencias en los protocolos de entrenamiento, estado de entrenamiento y tipo y cantidad de suplementación, así como también la redundancia inherente en los mecanismos que rigen las adaptaciones al ejercicio del musculo esquelético, pueden ser los factores responsables de la variabilidad en los resultados. La producción de ROS es solo uno de los mecanismos por los cuales se regula la adaptación, junto con cambios inducidos por la contracción en la tensión mecánica, la recuperación del ATP, el flujo de calcio, el equilibrio redox y la presión de oxígeno intracelular (Figura 2) [3]. Aunque muchos estudios observaron niveles atenuados de moléculas de señalización involucradas en la biogénesis mitocondrial, niveles elevados de actividad de CS sugieren que los cambios en el volumen mitocondrial no son inhibidos por la suplementación con antioxidantes [123 ,159]. Las investigaciones futuras deberían intentar diferenciar entre los efectos de un determinado suplemento de antioxidantes y las otras vías de señalización (por ejemplo, AMPK, SIRT1) que pueden verse influenciadas.
|
|
Suplemento | Dosis de suplementación | Participantes | Estado de entrenamiento | Duración | Tipo de entrenamiento | Cantidad total de sesiones de entrenamiento | Rendimiento (comparación con el grupo que consumió un placebo) | Adaptaciones metabólicas (comparación con el grupo que consumió un placebo) | Estrés oxidativo (comparación con el grupo que consumió un placebo) |
| Estudios con seres humanos | ||||||||||
| Sharman et al.
[114] |
Vitamina E | 400 mg | 26 m | Entrenados | 6 semanas | 4x/sem entrenamiento en natación competitivo no especificado | 24 | No se observaron diferencias en los tiempos de carrera de 1 min ni en los de nado de 400m | ||
| Lawrence et al.
[115] |
Vitamina E | 900 UI | 48 | Bien entrenados | 6 meses | Entrenamiento de natación competitivo, no especificado | No especificado | No se observaron diferencias en los tiempos de nado de 500 yd ni de 100 yd. | ||
| Rokitzki et al.
[116] |
Vitamin E | 330 mg | 30 m | Bien entrenados | 5 meses | Entrenamiento de ciclismo competitivo, no especificado | No especificado | No se observaron diferencias en el LT | Menor MDA | |
| Oostenbug
et al. [117] |
Vitamina E y aceite de pescado | 300 UI | 24 m | Bien entrenado | 3 semanas | Entrenamiento de ciclismo competitivo, no especificado | No especificado | No se observaron diferencias en VO2max, en la carga de trabajo máxima ni en la prueba contrarreloj de 1 hora | ||
| Gomez-
Cabrera et al. [118 |
Vitamina C | 1000 mg | 14 m | Sedentarios | 8 semanas | 3x/sem; 40 min ciclismo en estado estable a 65-80% VO2max. | 24 | Tendencia hacia una pequeña mejora en VO2max; +10,7 vs 22% (d = − 1.1,
[95% CI − 2.2, 0.04]) |
||
| Roberts et al.
[120] |
Vitamina C | 1000 mg | 15 m | Activos recreacionales | 4 semanas | 4x/sem HIIT; carrera en cinta rodante 5×3 min a 90%, 3 min de RBI | 16 | Ninguna diferencia en VO2max ni en el rendimiento en contrarreloj de 10 km. | Ninguna diferencia en el uso de sustratos | |
| Braakhuis
et al. [119] |
Vitamina C | 1000 mg | 23 f | Entrenados | 3 semanas | 3x/sem carrera; 4x 3-5 min y 6×2 min repeticiones cuesta arriba | 10 | No se observaron diferencias en la prueba contrarreloj de 5 km | Aumento en carbonilos proteicos en reposo, Mayor actividad de la SOD post-ejercicio, atenuación de la disminución inducida por el entrenameinto en la actividad CAT | |
| Bryant et al.
[121] |
Vitamina C y E | 1000 mg de vit C, 400 UI/kg de vit E, o 1000 mg de vit C+200 UI/kg de vit E | 7 m | Entrenados | 3 semanas | Entrenamiento de ciclismo competitivo, 250-350 km/sem | No especificado | No se observaron diferencias en el trabajo realizado | No se observaron diferencias en la oxidación de sustratos | La vitamina C aumentó MDA, no se observaron diferencias con el grupo Vit C+E |
| Ristow et al. [127] | Vitamina C y E | 1000 mg de vit C, 400 UI de vit E | 39 m | Entrenados y desentrenados | 4 semanas | 5x/sem; 20 min de ciclismo o carrera, 40 min de entrenamiento en circuito | 20 | Disminución en PGC-1ª; PGC-1β, PPARγ, SOD, y GPx | ||
| Yfanti et al.
[123,124] |
Vitamina C y E | 500 mg de vit C, 400 UI vit E | 21 m | Activos recreacionales | 12 semanas | 5x/sem ciclismo; 1 día de prueba de esfuerzo progresivo ; 10 x 3 min a 85% PPO, a min RBI; 1x 60 min a 60% PPO; 5 x 8 min a75% PPO; 4 min RBI; 1×120 min a 55%PPO | 60 | No se observaron diferencias en el VO2max, en la carga de trabajo máxima ni en LT. | No se observaron diferencias en CS, β-HAD, PGC-1ª ni enPPARγ | No se observaron diferencias en SOD |
| Paulsen et al.
[122] y Cumming et al. [126] |
Vitaminas C y E | 1000 mg vit C, 235 mg vit E | 26 m, 28 f | Entrenados | 11 semanas | 3-4 sem/sem de carrera; estado estable 2 días 30-60 min a 72-87% HRmax, 2 días 4-6x 4-6 min >90% HRmax. | 41 | No se observaron diferencias en VO2max ni en el test de ida y vuelta | Disminución en PGC-1α y en COX-IV | Disminución en el acido úrico
No se observaron diferencias en GPx, SOD, GSH ni en HSP70 |
| Morrison et al.
[125] |
Vitamina C y E | 1000 mg vit C, 400 UI vit E | 11 m | Activos recreacionalmente | 4 semanas | 3x/sem ciclismo, 10x 4 min a 90% VO2max, 2 min RBI | 12 | No se observaron diferencias en VO2max | No se observaron diferencias en
CS ni en COX-IV Menor TFAM |
Disminución en la actividad de SOD |
| Shill et al.
[193] |
Coenzima Q10 | 10 mg MitoQ (Marca registrada de suplemento de CoQ10) | 20 m | Activos recreacionales | 3 semanas | 3-5x/sem ciclismo 45-60 min a 50-70% de VO2max. | 13 | No se observaron diferencias en VO2max | No se observaron diferencias en la función mitocondrial | No se observaron diferencias en MDA |
| Ichinose et al.
[109] |
Extracto de te verde | 578 mg de te verde | 20 m | Activos recreacionales | 10 semanas | 3x/sem ciclismo, 60 min a 60% de VO2max | 30 | Mayor utilización de las grasas | ||
| Kuo et al.
[153] |
Extracto de te verde | 207 mg de catequinas de te | 40 m | Sedentarios | 4 semanas | 3x/sem de carrera, 20 min a 75% de la reserva de consumo de oxígeno | 12 | No se observaron diferencias en VO2max ni en el tiempo hasta el agotamiento | No se observaron diferencias en MDA ni en el estado antioxidante total | |
| Scribbans et al.
[147] |
Resveratrol | 150 mg | 16 m | Activos recreacionales | 4 semanas | 3x/sem HIIT de ciclismo, 8x 20 s a 170% PPO, 10s RBI | 12 | No se observaron diferencias en VO2max, en potencia aeróbica máxima, ni en la potencia en Wingate | No se observaron diferencias en la actividad de la succinato deshidrogenasa. Menor expresión génica de
PGC-1a, SIRT1, y SOD |
|
| Gliemann et al.
[145] y Oleson et al [145]. |
Resveratrol | 250 mg | 27 m | Sedentarios | 8 semanas | 2x/sem de HIIT de ciclismo, 1x/sem Crossfit (no especificado) | 24 | Pequeño incremento en VO2max:+12,8 vs. 17,2 % (d =−1,4,
[95% CI – 2,2, −0,5]). No se observaron diferencias en el tiempo hasta el agotamiento |
No se observaron diferencias en PGC-
1a mRNA, ni en las actividades de CYT-C, CS o β-HAD. |
Aumento en los carbonilos proteicos |
| Polley et al.
[194] |
Resveratrol | 500 mg de resveratrol + 10 mg de piperina | 9m, 7 f | Activos recreacionales | 4 semanas | 3x/sem, 30 min de ejercicios para los flexores de antebrazos y muñecas | 12 | Mayor capacidad oxidativa mitocondrial | ||
| Schwarz et al.
[157] |
Epicatequina | 200 mg | 20 m f | Activos recreacionales | 4 semanas | 4x/sem ciclismo, 2x 45-60 min a 50% Wmax, 1x/sem HIIT, 1x/sem SIT | 16 | Pequeño incremento en VO2max: +6,1 vs. 22,6 % (d=−0.6,
[95% CI – 1,5, 0,4]), ninguna diferencia en potencia aeróbica máxima |
Solo el placebo presentó un incremento en la actividad de la succinato deshidrogenasa (+59%) | |
| Animales | ||||||||||
| Venditti et al.
[128] |
Vitamina E | 700 mg/kg | 32m | Ratas | 10 sem | 5x/sem: 15-60 min/día natación | 50 | Disminución en la respiración mitocondrial, NRF-1, NRF-
2, PGC-1 |
Aumento de carbonilos proteicos. Menor actividad de la GPx, glutatión reductasa | |
| Asha Devi
et al. [134] |
Vitamina E | 50 UI/kg | 46 m | Ratas | 12 sem | 5x/sem: 5-30 min/ día natación con una carga de 3% de peso corporal adosada en la cola | 60 | Tiempo hasta el agotamiento:+33% | ||
| Kim et al.
[132] |
Vitamina C | 500 mg/kg | 24 m | Ratas | 4 semanas | 5x/sem; 2 sesiones/día natación 3 h por sesión, 45 min descanso entre sesiones | 40 | Ninguna diferencia en el tiempo hasta el agotamiento | No se observaron diferencias en la fosforilación de p38 MAPK y AMPK, o niveles de PGC-
1a, NRF-1, TFAM |
Disminución en la sustancias reactivas al acido tiobarbiturico (TBARS). |
| Gomez-
Cabrera et al. [118] |
Vitamina C | 500 mg/kg | 24 m | Ratas | 6 semanas | 5x/sem; 85 min/día carrera en cinta rodante a 75 % del VO2max | 30 | Tiempo hasta el agotamiento: +27 vs.187% (d=− 19,1,
[95% CI – 26,8, − 11,4]). Tendencia a un menor aumento en VO2max: +4,6 vs 7.1% (d=−0,9, [95%CI−2,1, 0,3]) |
||
| Higashida
et al. [131] |
Vitaminas C y E | 750 mg/kg vit
C, 150 mg/g vit E |
18 m | Ratas | 3 semanas | 6x/ sem; 2 sesiones/día de nado con 3 h por sesión y 45 min de descanso entre sesiones | 36 | No se observaron diferencias en las enzimas mitocondriales | Disminución en las TBARS
Ausencia de diferencia en SOD1 o SOD2 |
|
| Meier et al.
[129] |
Vitamins C,
coenzima Q10, N-acetilcisteina |
140 mg/l vit
C, 12 mg/l de co-Q10 y 1% NAC |
32 m | Ratones | 4 semanas | 5x/sem; 45 min de carrera en cinta rodante | 20 | Ausencia de diferencia en potencia máxima | Ausencia de diferencia en CS.
Menor expresión de SOD1, PGC 1ª o CD36 Mayor expresión de FABP-3 |
|
| Abadi et al.
[133] |
Vitamina E, coenzima Q10, acido alfa lipoico | Porción estándar con vitamina E (a-tocoferol,
1000 UI), 0,1% a-ácido lipoico, y 0.25% CoQ10 |
36 m, 36f | Ratones | 7 semanas | 3x/sem; 30-45 min de carrera en cinta rodante | 21 | No se observaron diferencias en el tiempo hasta el agotamiento | No se observaron diferencias en la capacidad respiratoria mitocondrial, CYT-C, PGC-1a | No se observaron diferencias en CAT, SOD1 ni en SOD2 |
| Strobel et al.
[130] |
Vitamina E, acido alfa lipoico | 1000 UI de Vit E/kg, 1,6 g/kg ALA | 48m | Ratas | 14 semanas | 4x/sem; 90 min carrera en cinta rodante a 70% VO2max | 56 | Disminución en PGC-
1a mRNA, PGC-1a y en la proteína COX IV , Menor actividad de la CS |
No se observaron diferencias en GPx, xantina oxidasa ni en MDA. | |
| Wadley et al.
[159] |
Allopurinol | 0,25 mg/ml | 24 m | ratas | 6 semanas | 5x/sem; 20-90 min de carrera en cinta rodante | 30 | Ausencia de diferencia en NRF-2, GLUT4 o en SOD mRNA ni en PGC-1ª, TFAM,CYT-C, CS y B-HAD | Ausencia de diferencias en SOD2 | |
| Lee et al. [158] | Epicatequina | 1 mg/kg, dos veces por día | 34 m | Ratones | 8 semanas | 5x/sem: 60 min de carrera en cinta rodante con una intensidad de 60% | 60 | Tiempo hasta el agotamiento: 84 vs. 45% (d= 18,0,
[95% CI 11,8, 24,3]) |
Mayor actividad de la CS, aumento en PGC-1B, TFAM. | |
| Dolinsky et al.
[195] |
Resveratrol | 4g/kg | 24 m | Ratas | 12 semanas | 5x/sem; 60 min carrera en cinta rodante | 60 | Tiempo hasta el agotamiento 21% mayor (d=1.5, [95%CI 0,5, 2,4]) | Mayor actividad CS, fosforilación de AMPK y expresión de PGC-1ª | |
| Hart et al. [149] | Resveratrol | 100 mg/kg | 24m | Ratas (alimentadas para lograr una mayor capacidad de resistencia) | 12 semanas | 5x/sem; 60 min de carrera en cinta rodante | 60 | VO2max: incremento de ~ 18%
(d = 2,4, [95% CI 0,9, 3,9]), Distancia de carrera 29% mayor durante el test de VO2max |
Mayor AMPK y SIRT1, disminución en PGC-1a | |
| Hart et al.
[150] |
Resveratrol | 100 mg/kg | 24 m | Ratas (alimentadas para lograr una baja capacidad de resistencia) | 12 semanas | 5x/sem; 60 min de carrera en cinta rodante | 60 | No se observaron diferencias en VO2max: | ||
| Kan et al.
[196] |
Resveratrol | 25 mg/kg | 16 m | Ratones | 4 semanas | 7x/sem: 30 min de natación | 28 | No se observaron diferencias en el tiempo de nado hasta el agotamiento | ||
| Murase et al.
[155] |
Extracto de te verde | 0,2–0,5% (wt/
wt) |
80 m | Ratones | 10 semanas | 2x/sem; 30 min nado | 20 | Tiempo hasta el agotamiento 24% mayor (d=2,3, [95%CI 1,2, 3,5]) | Mayor beta-oxidación. | |
| Murase et al.
[152] |
Extracto de te verde | 0,2–0,5(wt/
wt) |
32 m | Ratones | 8 semanas | 3x/sem; carrera en cinta rodante de 30 min | 24 | Tiempo hasta el agotamiento 30 % mayor (d=1.9, [95%CI 0,7, 3,0]) | Mayor beta-oxidación | |
Tabla 4. Descripción de los estudios que analizaron la suplementación con antioxidantes durante entrenamiento de la resistencia supervisado. Tamaño de efecto de los suplementos calculado con d de Cohen en aquellos datos que estuvieran disponibles (informado como tamaño de efecto, 95% CI): HIIT = entrenamiento intervalado de alta intensidad; SIT= entrenamiento intervalado de esprint; TTE= Tiempo hasta el agotamiento; PPO= producción de potencia máxima; RBI= descanso entre intervalos; RBS= descanso entre series; HR= Frecuencia cardíaca.
Cafeína
La cafeína ha sido ampliamente estudiada y comúnmente se informa que sus efectos mejoran el rendimiento durante el ejercicio de resistencia [160]. Cuando se toma en dosis moderadas (3–6 mg /kg), se han observado mejoras de 2–3% en el rendimiento de pruebas contrarreloj que tenían una duración de 6 min a 2,5 h [ 160] y en la potencia durante HIIT [161]. Se ha sugerido que el consumo habitual de cafeína disminuiría su eficacia [162]. Sin embargo, la suplementación con cafeína (4–6 mg/kg) mejoró el rendimiento de la prueba contrarreloj de ciclismo de 30 a 45 minutos con consumos habituales de cafeína bajos, moderados y altos [163 ,164 ], y la ingesta de 3 mg/kg durante 20 días continuó produciendo un efecto ergogénico [165], lo que sugiere que el consumo regular de cafeína durante las sesiones de entrenamiento no debe reducir su impacto a largo plazo. A pesar de uso extendido, se sabe poco sobre los efectos de la ingesta de cafeína previa al ejercicio en las adaptaciones al entrenamiento subsiguiente.
Hay varios mecanismos que podrían conducir a mejores adaptaciones al entrenamiento de resistencia. Gracias a la reducción en la percepción de esfuerzo, probablemente a través de sus efectos como un antagonista de receptores de adenosina [166 ], un atleta puede ser capaz de acumular un mayor estrés de entrenamiento. De hecho, los participantes que consumieron 3–6 mg/kg de cafeína realizaron un 12,6% más de trabajo durante 30 minutos de ciclismo a un nivel dado de esfuerzo percibido [167], aumentaron la potencia un 2,8% durante HIIT (8×5 min a intensidad máxima con 1 min de recuperación) [161], y pudieron mitigar las reducciones de potencia durante las sesiones de entrenamiento realizadas con baja disponibilidad de carbohidratos [161]. La cafeína puede aumentar la oxidación exógena de carbohidratos [168], posiblemente a través de una mayor absorción intestinal [169], y también aumentar la activación de AMPK a través de la actividad de la proteína fosfatasa 2A mediada por calcio [170]. Las ultimas investigaciones también apuntas a que la cafeína participaría en la mejora de la respiración mitocondrial a través de su efectos sobre la p27 mitocondrial [171], sugiriendo el potencial de trabajar sinérgicamente con SIT (la forma de entrenamiento intervalado que se ha asociado con las mayores mejoras en la respiración mitocondrial) [172]. Teniendo en cuenta todo esto, la cafeína tiene el potencial de afectar las adaptaciones al entrenamiento a través de varias vías claves que, en última instancia, pueden conducir a una mayor aumentos en la biogénesis mitocondrial (Figura 2).
A pesar de la justificación anterior, solo un estudio realizado en humanos, y un estudio realizado con ratas, investigaron los efectos de la cafeína sobre las adaptaciones al entrenamiento de resistencia. En el estudio realizado con seres humanos, la cafeína formaba parte de un suplemento con múltiples ingredientes, no se controló la ingesta dietaria de cafeína y no hubo diferencias en el consumo de cafeína entre los grupos [173], mientras que en el estudio realizado con ratas, las mismas recibieron cafeína antes de cada sesión de ejercicio durante 6 semanas de HIIT pero solo se estudiaron los cambios en los marcadores biológicos cerebrales y conductuales [174]. Las futuras investigaciones deberían analizar los efectos de la cafeína en las adaptaciones al entrenamiento, junto con el efecto en la intensidad del ejercicio, el estado de entrenamiento [175 ], sexo [176 ] y genotipo [177], usando dosis moderadas (3–6 mg / kg) y bajas (<3 mg / kg) [ 178].
Creatina
Aunque la suplementación con creatina rara vez se asocia con deportes de resistencia, se ha demostrado que mejora el rendimiento en los ejercicios a través de una variedad de eventos deportivos (por ejemplo, carreras de velocidad, distancia media, deportes de equipo y HIIT en deportes de resistencia [179]) y esto ha sido atribuido a un mayor contenido muscular de creatina y fosfocreatina [179]. Una dosis de 5 g cuatro veces al día durante 5-7 días se utiliza comúnmente dentro de los protocolos de carga, con dosis diarias subsiguientes de 3-5 g/día para mantener niveles elevados de creatina [179]. Sin embargo, se han identificado buenos y malos respondedores a la suplementación con creatina, posiblemente debido a variaciones en el contenido de creatina muscular basal [180], y/o a su captación y uso [181 ]. A pesar del rol reconocido de la creatina para mejorar el rendimiento, existen pocas investigaciones sobre su capacidad de afectar las adaptaciones al entrenamiento.
Existen varios mecanismos potenciales por los cuales la suplementación con creatina puede afectar el las adaptaciones al entrenamiento. La intensidad del ejercicio sería un factor clave para aumentos inducidos por el entrenamiento en la respiración mitocondrial [172], y por lo tanto cualquier suplemento que permita aumentar la intensidad del ejercicio podría ofrecer beneficios adicionales para el entrenamiento la adaptación y el rendimiento de resistencia. Además de su función principal de combinarse con un grupo fosforilo para formar fosforilcreatina a través de la reacción catalizada por la creatina quinasa, la creatina también puede desempeñar un papel en el metabolismo de energía aeróbico mediante la conexión de sitios de producción de ATP (glucolisis y fosforilación oxidativa) con los sitios subcelulares donde se utiliza ATP (ATPasas) [182], con la subsiguiente mejora en la respiración mitocondrial en las fibras de contracción lenta pero no en las fibras de contracción rápida [183]. Esto permitiría realizar una mayor cantidad de trabajo durante una sesión de entrenamiento, y un menor costo de oxígeno durante el ejercicio submáximo. También se ha demostrado que la creatina tiene efectos antioxidantes a través de la reducción en la formación de ROS, de la reducción del daño oxidativo del ADN y de la peroxidación lipídica después del ejercicio, lo que podría afectar la señalización celular inducida por el ejercicio [184]. Existe la posibilidad de un incremento en la masa corporal debido a la retención de agua que se produce con la carga de creatina [179]. Sin embargo, a pesar de un aumento de ~ 2,5% en la masa corporal, ciclistas bien entrenados sometidos a carga de creatina y de carbohidratos presentaron una mayor producción de potencia durante los esfuerzos de esprint en una contrarreloj simulada de 120 km, pero no presentaron diferencias con el grupo que consumió el placebo en el ejercicio de simulación de ciclismo cuesta arriba [185].
Dos estudios realizados con varones recreacionalmente activos que realizaron 4 semanas de HIIT mientras consumían un suplemento con creatina (10 g/día) o un placebo observaron mejoras significativas en el grupo que consumió creatina pero no en el grupo que consumió el placebo en variables como potencia crítica y umbral ventilatorio (Tabla 5) [186, 187]. Sin embargo, no se observaron diferencias entre los grupos en VO2max, tiempo hasta el agotamiento en VO2max , capacidad de trabajo anaeróbico ni en el trabajo total realizado durante una prueba de ciclismo hasta el agotamiento al 110% de la potencia aeróbic máxima [186, 187]. Investigaciones similares realizadas con mujeres activas recreacionalmente no observaron diferencias en las mejoras inducidas por el ejercicio en VO2max, en el umbral ventilatorio o en rendimiento contrarreloj de 2 km (~ 2 min) [188]. Sin embargo, este estudio no contempló la equiparación de fase menstrual, algo que se ha demostrado que afecta la respuesta del lactato sanguíneo en el ejercicio de alta intensidad [189]. Al igual que otros suplementos, es difícil separar los efectos de la creatina en el rendimiento a partir de sus efectos sobre las adaptaciones al entrenamiento. Por ejemplo, en ausencia de entrenamiento, 5-7 días de carga con creatina provocaron aumentos de la potencia en el umbral de lactato [190] y en el tiempo supra-máximo hasta el agotamiento [190 ,191], así como también un VO2 más bajo durante el ciclismo sub-máximo [191]. Por lo tanto, mientras que la creatina puede mejorar algunas adaptaciones al entrenamiento de resistencia, la evidencia limitada aún no es compatible con su uso generalizado por atletas de resistencia. Se necesita más investigación, particularmente en participantes que realizan intervalos de 15 segundos a 4 minutos usando esfuerzos máximos en lugar de tasas de trabajo predeterminadas, y que también aseguren la medición de los efectos del suplemento solo (Tabla 2).
| Participantes | Estado de entrenamiento | Duración (semanas) | Dosis de suplementación | Tipo de entrenamiento | Cantidad total de sesiones de entrenamiento | Rendimiento (comparado con el grupo placebo) | |
| Graef et al. [187] | 33 m | Activos recreacionales | 4 | 10 g/día durante los primeros 10 días,
luego 10 g/día 5 ×/sem durante 5 semanas (solo los días de entrenamiento) |
Entrenamiento 5/sem; 3/sem HIIT, 5×2 min a 90–120%
PPO, 1 min RBI; recuperación 2 ×/sem, 5 × 2 min a 80% PPO, 1 min RBI |
20 | Umbral ventilatorio: +16% vs 10 % (d = 0.2, [95% CI – 0.5, 0.9])
No se observaron diferencia en VO2max, ni en TTE en VO2max. |
| Kendall et al. [186] | 42 m | Activos recreacionales | 4 | 10 g/día durante los primeros 10 días,
luego 10 g/día 5 ×/sem durante 3 semanas (solo los días de entrenamiento) |
Entrenamiento 5/sem; 3/sem HIIT, 5-6 × 2 min a 90–120%
PPO, 1 min RBI; recuperación 2 ×/sem, 5 × 2 min a 80% PPO, 1 min RBI |
20 | Potencia crítica (w): + 6,7% vs. ningún cambio en el control (d = 0,1,
[95% CI – 0,6, 0,8]) No se observaron cambios en la capacidad de realizar trabajo aeróbico |
| Forbes et al. [188] | 17 f | Activos recreacionales | 4 | 0,3 g/kg peso corporal/ día durante
5 días y luego 0,1 g/kg peso corporal durante 23 días. |
HIIT 3 ×/sem; 1 sesión de 4–6 Tests de Wingate , 4 min
RBI; 1 sesión de 10–20 esprints de 6 s, 24 s de recuperación; 1 sesión de 8–12 × 60 s a 85% y 60 s a 15% PPO |
12 | No se observaron diferencias en VO2max, LT ni en el rendimiento de pruebas contrarreloj. |
Tabla 5. Generalidades de los estudios que utilizaron suplementación con creatina durante entrenamiento de resistencia supervisado. Tamaño de efecto de los suplementos calculado con d de Cohen en aquellos datos que estuvieran disponibles (informado como tamaño de efecto, 95% CI): HIIT = entrenamiento intervalado de alta intensidad; TTE= Tiempo hasta el agotamiento; PPO= producción de potencia máxima; RBI= descanso entre intervalos.
Conclusión
Las variables más importantes que afectan las adaptaciones al entrenamiento de resistencia son el volumen y la intensidad del estímulo de entrenamiento. Sin embargo, dentro de un paradigma de entrenamiento dado, el uso apropiado de suplementos dietéticos puede ofrecer más beneficios. Estos beneficios permitirían en gran medida manejar una mayor intensidad de entrenamiento, por lo que las prescripciones de HIIT deberían evitar cargas de trabajo predeterminadas a favor de intervalos basados en el tiempo (por ejemplo, esfuerzos máximos de 4 minutos). El uso de bicarbonato de sodio y β-alanina tienen potencial para permitir una mayor adaptación al entrenamiento, particularmente cuando los estímulos de ejercicio son suficiente para alterar los niveles de lactato y/o el pH en comparación con un placebo. El jugo de remolacha parece afectar la remodelación del tipo de fibra del músculo esquelético, aunque es necesario realizar más investigaciones con entrenamiento de la resistencia concurrente. Dosis suprafisiológicas de antioxidantes deben usarse con precaución ya que la investigación no es clara con respecto al alcance de sus efectos en las adaptaciones al entrenamiento, pero parece poco probable que afecten negativamente el rendimiento a corto plazo (<6 meses). La cafeína y la creatina tienen potencial para aumentar las adaptaciones al entrenamiento de resistencia, aunque carecemos de datos claros.
Finalmente, es imprescindible que los atletas que compiten bajo reglas antidopaje eviten suplementos que contengan sustancias prohibidas [192]. Es tentador interpretar efectos pequeños o triviales observados en la ciencia deportiva como potencialmente inocuos, y es necesario sopesar el riesgo de presentar pruebas de dopaje positivas con los efectos no comprobados de un suplemento. Claramente, hay que tener mucha precaución cuando los atletas, entrenadores y el personal médico seleccionan los suplementos dietarios que pueden ser consumidos.
Cumplimiento de normas éticas
Financiamiento: No se utilizaron fuentes de financiamiento para ayudar en la preparación de este artículo
Conflicto de intereses Jeffrey Rothschild y David Bishop declaran que no tienen conflictos de interés relacionados con el contenido de esta revisión.
Version original: Jeffrey A. Rothschild and David J. Bishop. (2019). Effects of Dietary Supplements on Adaptations to Endurance Training. Sports Medicine. https://doi.org/10.1007/s40279-019-01185-8
REFERENCIAS
- Hawley JA. Adaptations of skeletal muscle to prolonged, intense endurance training. Clin Exp Pharmacol Physiol. 2002;29(3):218–22.
- Holloszy JO, Coyle EF. Adaptations of skeletal muscle to endur- ance exercise and their metabolic consequences. J Appl Physiol Respir Environ Exerc Physiol. 1984;56(4):831–8. https://doi. org/10.1152/jappl.1984.56.4.831.
- Egan B, Zierath JR. Exercise metabolism and the molecu- lar regulation of skeletal muscle adaptation. Cell Metab.2013;17(2):162–84.
- Perry CG, Lally J, Holloway GP, Heigenhauser GJ, Bonen A, Spriet LL. Repeated transient mRNA bursts precede increases in transcriptional and mitochondrial proteins during training in human skeletal muscle. J Physiol. 2010;588(23):4795–810.
- Seiler S. What is best practice for training intensity and duration distribution in endurance athletes? Int J Sports Physiol Perform. 2010;5(3):276–91.
- Rothschild J, Earnest CP. Dietary manipulations concurrent to endurance training. J Funct Morphol Kinesiol. 2018;3(3):41.
- Knapik JJ, Steelman RA, Hoedebecke SS, Austin KG, Farina EK, Lieberman HR. Prevalence of dietary supplement use by athletes: systematic review and meta-analysis. Sports Med. 2016;46(1):103–23.
- Lancha Junior AH, Painelli Vde S, Saunders B, Artioli GG. Nutritional strategies to modulate intracellular and extracellular buffering capacity during high-intensity exercise. Sports Med. 2015;45(Suppl 1):S71–81. https://doi.org/10.1007/s4027 9-015-0397-5.
- Saunders B, Elliott-Sale K, Artioli GG, Swinton PA,Dolan E, Roschel H, et al. beta-alanine supplementation to improve exercise capacity and performance: a systematic review and meta-analysis. Br J Sports Med. 2017;51(8):658–69. https://doi. org/10.1136/bjsports-2016-096396.
- Domínguez R, Cuenca E, Maté-Muñoz JL, García-Fernández P, Serra-Paya N, Estevan MCL, et al. Effects of beetroot juice supplementation on cardiorespiratory endurance in athletes. A systematic review. Nutrients. 2017;9(1):43.
- Jones AM. Influence of dietary nitrate on the physiological determinants of exercise performance: a critical review. Appl Physiol Nutr Metab. 2014;39(9):1019–28. https://doi.org/10.1139/ apnm-2014-0036.
- Peeling P, Binnie MJ, Goods PSR, Sim M, Burke LM. Evidence- based supplements for the enhancement of athletic performance. Int J Sport Nutr Exerc Metab. 2018;28(2):178–87. https://doi. org/10.1123/ijsnem.2017-0343.
- Christensen PM, Shirai Y, Ritz C, Nordsborg NB. Caffeine and bicarbonate for speed. A meta-analysis of legal supplements potential for improving intense endurance exercise perfor- mance. Front Physiol. 2017;8:240. https://doi.org/10.3389/fphys.2017.00240.
- Nikolaidis MG, Kerksick CM, Lamprecht M, McAnulty SR. Does vitamin C and E supplementation impair the favorable adaptations of regular exercise? Oxid Med Cell Longev. 2012;2012:707941. https://doi.org/10.1155/2012/707941.
- Gibala MJ, Gillen JB, Percival ME. Physiological and health- related adaptations to low-volume interval training: influences of nutrition and sex. Sports Med. 2014;44(Suppl 2):S127–37. https://doi.org/10.1007/s40279-014-0259-6.
- McNaughton LR, Gough L, Deb S, Bentley D, Sparks SA. Recent developments in the use of sodium bicarbonate as an ergogenic Curr Sports Med Rep. 2016;15(4):233–44.
- Hayashi T, Shigetomi T, Ueda M, Kaneda T, Matsumoto T, Tokuno H, et al. Effects of ammonium chloride on membrane currents of acinar cells dispersed from the rat parotid gland. Pflug Arch. 1992;420(3–4):297–301.
- Stathopoulou K, Gaitanaki C, Beis I. Extracellular pH changes activate the p38-MAPK signalling pathway in the amphibian heart. J Exp Biol. 2006;209(Pt 7):1344–54. https://doi. org/10.1242/jeb.02134.
- Genders AJ, Martin SD, McGee SL, Bishop DJ. A physiological drop in pH decreases mitochondrial respiration, and HDAC and Akt signaling, in L6 myocytes. Am J Physiol Cell Physiol. 2019;316(3):C404–14. https://doi.org/10.1152/ajpcell.00214.2018.
- Balgi AD, Diering GH, Donohue E, Lam KK, Fonseca BD, Zimmerman C, et al. Regulation of mTORC1 signaling by pH. PLoS One. 2011;6(6):e21549. https://doi.org/10.1371/journpone.0021549.
- Zhao L, Cui L, Jiang X, Zhang J, Zhu M, Jia J, et al. Extracel- lular pH regulates autophagy via the AMPK–ULK1 pathway in rat cardiomyocytes. FEBS Lett. 2016;590(18):3202–12. https://org/10.1002/1873-3468.12359.
- Edge MT, Pilegaard H, Hawke E, Leikis M, Lopez-Villa- lobos N, et al. Ammonium chloride ingestion attenuates exercise-Induced mRNA levels in human muscle. PLoS One. 2015;10(12):e0141317. https://doi.org/10.1371/journpone.0141317.
- Correia-Oliveira CR, Kiss MAPDM. Induced metabolic aci- dosis by ammonium chloride: action mechanisms, dose and effects on athletic performance. J Phys Educ. 2017. https://doi. org/10.4025/jphyseduc.v28i1.2860.
- Hashimoto T, Hussien R, Oommen S, Gohil K, Brooks GA. Lactate sensitive transcription factor network in L6 cells: activation of MCT1 and mitochondrial biogenesis. FASEB J. 2007;21(10):2602–12. https://doi.org/10.1096/fj.07-8174com.
- Preobrazenski N, Bonafiglia JT, Nelms MW, LuS, Robins L, LeBlanc C, et al. Does blood lactate predict the chronic adaptive response to training: a comparison of traditional and talk test prescription methods. Appl Physiol Nutr Metab.2018;44(2):179–86.
- Hollidge-Horvat MG, Parolin ML, Wong D, Jones NL, Heigenhauser GJ. Effect of induced metabolic alkalosis on human skeletal muscle metabolism during exercise. Am J Physiol Endo- crinol Metab. 2000;278(2):E316–29. https://doi.org/10.1152/2000.278.2.E316.
- Percival ME, Martin BJ, Gillen JB, Skelly LE, MacInnis MJ, Green AE, et al. Sodium bicarbonate ingestion augments the increase in PGC-1α mRNA expression during recovery from intense interval exercise in human skeletal muscle. J Appl Phys 2015;119(11):1303–12.
- Cochran AJ, Percival ME, Tricarico S, Little JP, Cermak N, Gillen JB, et al. Intermittent and continuous high-intensity exercise training induce similar acute but different chronic muscle adapta- Exp Physiol. 2014;99(5):782–91.
- Burke LM, Pyne DB. Bicarbonate loading to enhance training and competitive performance. Int J Sports Physiol Perform.2007;2(1):93–7.
- Jones RL, Stellingwerff T, Artioli GG, Saunders B, Cooper S, Sale C. Dose-response of sodium bicarbonate ingestion high- lights individuality in time course of blood analyte responses. Int J Sport Nutr Exerc Metab. 2016;26(5):445–53. https://doi. org/10.1123/ijsnem.2015-0286.
- Froio de Araujo Dias G, da Eira Silva V, de Salles Painelli V, Sale C, Giannini Artioli G, Gualano B, et al. (In)consistencies in responses to sodium bicarbonate supplementation: a randomised, repeated measures, counterbalanced and double-blind study. PLoS One. 2015;10(11):e0143086. https://doi.org/10.1371/journpone.0143086.
- Gough LA, Deb SK, Sparks AS, McNaughton LR. The reproduc- ibility of blood acid base responses in male collegiate athletes following individualised doses of sodium bicarbonate: a randomised controlled crossover study. Sports Med. 2017;47(10):2117–27. https://doi.org/10.1007/s40279-017-0699-x.
- Edge J, Bishop D, Goodman C. Effects of chronic NaHCO3 ingestion during interval training on changes to muscle buffer capacity, metabolism, and short-term endurance performance. J Appl Physiol. 2006;101(3):918–25.
- Wang J, Qiu J, Yi L, Hou Z, Benardot D, Cao W. Effect of sodium bicarbonate ingestion during 6 weeks of HIIT on anaerobic performance of college students. J Int Soc Sports Nutr. 2019;16(1):18. https://doi.org/10.1186/s12970-019-0285-8.
- Hawke E, Hammarström D, Sahlin K, Tonkonogi M. Does six- weeks of high-intensity cycle training with induced changes in acid-base balance lead to mitochondrial adaptations? J Sci Cycl. 2014;3(2):82.
- Driller MW, Gregory JR, Williams AD, Fell JW. The effects of chronic sodium bicarbonate ingestion and interval train- ing in highly trained rowers. Int J Sport Nutr Exerc Metab. 2013;23(1):40–7.
- Bishop DJ, Thomas C, Moore-Morris T, Tonkonogi M, Sahlin K, Mercier J. Sodium bicarbonate ingestion prior to training improves mitochondrial adaptations in rats. Am J Physiol Endocrinol Metab. 2010;299(2):E225–33.
- Thomas C, Bishop D, Moore-Morris T, Mercier J. Effects of high-intensity training on MCT1, MCT4, and NBC expressions in rat skeletal muscles: influence of chronic metabolic alkalo- sis. Am J Physiol Endocrinol Metab. 2007;293(4):E916–22.
- Lundby C, Montero D, Joyner M. Biology of VO2max: looking under the physiology lamp. J Acta Physiologica.2017;220(2):218–28.
- Stellingwerff T, Anwander H, Egger A, Buehler T, Kreis R, Decombaz J, et al. Effect of two β-alanine dosing protocols on muscle carnosine synthesis and washout. Amino Acids. 2012;42(6):2461–72.
- Stout JR, Cramer JT, Zoeller RF, Torok D, Costa P, Hoffman JR, et al. Effects of beta-alanine supplementation on the onset of neuromuscular fatigue and ventilatory threshold in women. Amino Acids. 2007;32(3):381–6. https://doi.org/10.1007/ s00726-006-0474-z.
- Hoffman JR, Ratamess NA, Faigenbaum AD, Ross R, Kang J, Stout JR, et al. Short-duration beta-alanine supplementation increases training volume and reduces subjective feelings of fatigue in college football players. Nutr Res. 2008;28(1):31–5. https://doi.org/10.1016/j.nutres.2007.11.004.
- Baguet A, Koppo K, Pottier A, Derave W. β-Alanine supple- mentation reduces acidosis but not oxygen uptake response during high-intensity cycling exercise. Eur J Appl Physiol. 2010;108(3):495–503.
- Gross M, Boesch C, Bolliger CS, Norman B, Gustafsson T, Hoppeler H, et al. Effects of beta-alanine supplementation and interval training on physiological determinants of severe exer- cise performance. Eur J Appl Physiol. 2014;114(2):221–34.https://doi.org/10.1007/s00421-013-2767-8.
- Glenn J, Gray M, Stewart R, Moyen N, Kavouras S, DiBrezzo R, et al. Incremental effects of 28 days of beta-alanine supplementation on high-intensity cycling performance and blood lactate in masters female cyclists. Amino Acids.2015;47(12):2593–600.
- Begum G, Cunliffe A, Leveritt M. Physiological role of car- nosine in contracting muscle. Int J Sport Nutr Exerc Metab. 2005;15(5):493–514.
- Boldyrev AA, Aldini G, Derave W. Physiology and pathophysiol- ogy of carnosine. Physiol Rev. 2013;93(4):1803–45. https://doi. org/10.1152/physrev.00039.2012.
- Hoetker D, Chung W, Zhang D, Zhao J, Schmidtke VK, Riggs DW, et al. Exercise alters and beta-alanine combined with exercise augments histidyl dipeptide levels and scavenges lipid per- oxidation products in human skeletal muscle. J Appl Physiol (1985). 2018. https://doi.org/10.1152/japplphysiol.00007.2018.
- Dutka TL, Lamboley CR, McKenna MJ, Murphy RM, Lamb GD. Effects of carnosine on contractile apparatus Ca2+ sensitivity and sarcoplasmic reticulum Ca2+ release in human skeletal muscle J Appl Physiol. 2011;112(5):728–36.
- Hannah R, Stannard RL, Minshull C, Artioli GG, Harris RC, Sale C. β-Alanine supplementation enhances human skeletal muscle relaxation speed but not force production capacity. J Appl Phys- 2014;118(5):604–12.
- Turcotte LP, Abbott MJ. Contraction-induced signaling: evidence of convergent cascades in the regulation of muscle fatty acid metabolism. Can J Physiol Pharmacol. 2012;90(11):1419–33. https://doi.org/10.1139/y2012-124.
- Schnuck JK, Sunderland KL, Kuennen MR, Vaughan RA. Characterization of the metabolic effect of β-alanine on markers of oxidative metabolism and mitochondrial biogenesis in skeletal J Exerc Nutr Biochem. 2016;20(2):34.
- Bellinger PM, Minahan CL. Additive benefits of beta-alanine supplementation and sprint-interval training. Med Sci Sports Exerc. 2016;48(12):2417–25. https://doi.org/10.1249/0000000000001050.
- Walter AA, Smith AE, Kendall KL, Stout JR, Cramer JT. Six weeks of high-intensity interval training with and without β-alanine supplementation for improving cardiovascular fitness in women. J Strength Cond Res. 2010;24(5):1199–207.
- Cochran AJ, Percival ME, Thompson S, Gillen JB, MacInnis MJ, Potter MA, et al. β-Alanine supplementation does not augment the skeletal muscle adaptive response to 6 weeks of sprint inter- val training. Int J Sport Nutr Exerc Metab. 2015;25(6):541–9.
- Wang R, Fukuda DH, Hoffman JR, La Monica MB, Starling TM, Stout JR, et al. Distinct effects of repeated-sprint training in normobaric hypoxia and beta-alanine supplementation. J Am Coll Nutr. 2018. https://doi.org/10.1080/07315724.2018.14752 69.
- Smith AE, Walter AA, Graef JL, Kendall KL, Moon JR, Lock- wood CM, et al. Effects of beta-alanine supplementation and high-intensity interval training on endurance performance and body composition in men; a double-blind trial. J Int Soc Sports 2009;6:5. https://doi.org/10.1186/1550-2783-6-5.
- Santana JO, de Freitas MC, Dos Santos DM, Rossi FE, Lira FS, Rosa-Neto JC, et al. Beta-alanine supplementation improved 10-km running time trial in physically active adults. Front Phys- 2018;9:1105. https://doi.org/10.3389/fphys.2018.01105.
- Howe ST, Bellinger PM, Driller MW, Shing CM, Fell JW. The effect of beta-alanine supplementation on isokinetic force and cycling performance in highly trained cyclists. Int J Sport Nutr Exerc Metab. 2013;23(6):562–70.
- Bellinger PM, Minahan CL. Metabolic consequences of β-alanine supplementation during exhaustive supramaximal cycling and 4000-m time-trial performance. Appl Physiol Nutr Metab. 2016;41(8):864–71.
- Bellinger PM, Howe ST, Shing CM, Fell JW. Effect of combined beta-alanine and sodium bicarbonate supplementation on cycling performance. Med Sci Sports Exerc. 2012;44(8):1545–51. https://doi.org/10.1249/MSS.0b013e31824cc08d.
- Hobson RM, Saunders B, Ball G, Harris R, Sale C. Effects of β-alanine supplementation on exercise performance: a meta- Amino Acids. 2012;43(1):25–37.
- Church DD, Hoffman JR, Varanoske AN, Wang R, Baker KM, La Monica MB, et al. Comparison of two beta-alanine dosing protocols on muscle carnosine elevations. J Am Coll Nutr. 2017;36(8):608–16. https ://doi.org/10.1080/073152017.1335250.
- Saunders B, Sale C, Harris RC, Sunderland C. Sodium bicarbonate and high-intensity-cycling capacity: variability in responses. Int J Sports Physiol Perform. 2014;9(4):627–32. https://doi. org/10.1123/ijspp.2013-0295.
- Naderi A, Earnest CP, Lowery RP, Wilson JM, Willems ME. Co-ingestion of nutritional ergogenic aids and high-intensity exercise performance. Sports Med. 2016;46(10):1407–18. https://doi.org/10.1007/s40279-016-0525-x.
- Painelli VS, Roschel H, Jesus F, Sale C, Harris RC, Solis MY, et al. The ergogenic effect of beta-alanine combined with sodium bicarbonate on high-intensity swimming performance. Appl Physiol Nutr Metab. 2013;38(5):525–32. https://doi.org/10.1139/ apnm-2012-0286.
- Danaher J, Gerber T, Wellard RM, Stathis CG. The effect of beta-alanine and NaHCO3 co-ingestion on buffering capacity and exercise performance with high-intensity exercise in healthy males. Eur J Appl Physiol. 2014;114(8):1715–24. https://doi. org/10.1007/s00421-014-2895-9.
- Sale C, Saunders B, Hudson S, Wise JA, Harris RC, Sun- derland CD. Effect of beta-alanine plus sodium bicarbonate on high-intensity cycling capacity. Med Sci Sports Exerc. 2011;43(10):1972–8. https://doi.org/10.1249/MSS.0b013e3182188501.
- Lundberg JO, Govoni M. Inorganic nitrate is a possible source for systemic generation of nitric oxide. Free Radic Biol Med. 2004;37(3):395–400.
- Rimer EG, Peterson LR, Coggan AR, Martin JC. Acute dietary nitrate supplementation increases maximal cycling power in Int J Sports Physiol Perform. 2016;11(6):715.
- Larsen FJ, Schiffer TA, Borniquel S, Sahlin K, Ekblom B, Lun- dberg JO, et al. Dietary inorganic nitrate improves mitochondrial efficiency in humans. Cell Metab. 2011;13(2):149–59. https://doi.org/10.1016/j.cmet.2011.01.004.
- Bailey SJ, Fulford J, Vanhatalo A, Winyard PG, Blackwell JR, DiMenna FJ, et al. Dietary nitrate supplementation enhances muscle contractile efficiency during knee-extensor exercise in humans. J Appl Physiol (1985). 2010;109(1):135–48. https://org/10.1152/japplphysiol.00046.2010.
- Hernandez A, Schiffer TA, Ivarsson N, Cheng AJ, Bruton JD, Lundberg JO, et Dietary nitrate increases tetanic [Ca2+] i and contractile force in mouse fast-twitch muscle. J Phys- iol. 2012;590(15):3575–83. https://doi.org/10.1113/jphys iol.2012.232777.
- Clementi E, Nisoli E. Nitric oxide and mitochondrial biogene- sis: a key to long-term regulation of cellular metabolism. Comp Biochem Physiol A Mol Integr Physiol. 2005;142(2):102–10. https://doi.org/10.1016/j.cbpb.2005.04.022.
- Thompson C, Wylie LJ, Blackwell JR, Fulford J, Black MI, Kelly J, et al. Influence of dietary nitrate supplementation on physiological and muscle metabolic adaptations to sprint inter- val training. J Appl Physiol (1985). 2017;122(3):642–52. https://doi.org/10.1152/japplphysiol.00909.2016.
- Martins KJ, St-Louis M, Murdoch GK, MacLean IM, McDon- ald P, Dixon WT, et al. Nitric oxide synthase inhibition pre- vents activity-induced calcineurin–NFATc1 signalling and fast-to-slow skeletal muscle fibre type conversions. J Phys- iol. 2012;590(6):1427–42. https://doi.org/10.1113/jphys2011.223370.
- De Smet S, Van Thienen R, Deldicque L, James R, Sale C, Bishop DJ, et al. Nitrate intake promotes shift in muscle fiber type composition during sprint interval training in hypoxia. Front Physiol. 2016;7:233. https://doi.org/10.3389/fphys.2016.00233.
- Whitfield J, Ludzki A, Heigenhauser GJ, Senden JM, Verdijk LB, van Loon LJ, et al. Beetroot juice supplementation reduces whole body oxygen consumption but does not improve indices of mitochondrial efficiency in human skeletal muscle. J Physiol. 2016;594(2):421–35. https://doi.org/10.1113/JP270844.
- Egan B, Carson BP, Garcia-Roves PM, Chibalin AV, Sarsfield FM, Barron N, et al. Exercise intensity-dependent regulationof peroxisome proliferator-activated receptor γ coactivator-1α mRNA abundance is associated with differential activation of upstream signalling kinases in human skeletal muscle. J Physiol. 2010;588(10):1779–90.
- Peeling P, Cox GR, Bullock N, Burke LM. Beetroot juice improves on-water 500 M time-trial performance, and labora- tory-based paddling economy in national and international-level kayak athletes. Int J Sport Nutr Exerc Metab. 2015;25(3):278–84. https://doi.org/10.1123/ijsnem.2014-0110.
- Croitoru MD, Fülöp I, Fogarasi E, Muntean D-L. Is nitrate a good biomarker of the nitric oxide status?/Este ionul nitrat un bun biomarker al producţiei endogene de monoxid de azot? Rev Rom Med Lab. 2015;23(1):127–35.
- Wylie LJ, Kelly J, Bailey SJ, Blackwell JR, Skiba PF, Win- yard PG, et al. Beetroot juice and exercise: pharmacodynamic and dose–response relationships. J Appl Physiol (1985). 2013;115(3):325–36. https://doi.org/10.1152/japplphysiol.00372.2013.
- Puype J, Ramaekers M, Van Thienen R, Deldicque L, Hespel P. No effect of dietary nitrate supplementation on endurance training in hypoxia. Scand J Med Sci Sports. 2015;25(2):234–41.
- Muggeridge DJ, Sculthorpe N, James PE, Easton C. The effects of dietary nitrate supplementation on the adaptations to sprint interval training in previously untrained males. J Sci Med Sport. 2017;20(1):92–7. https://doi.org/10.1016/j.jsams.2016.04.014.
- Thompson C, Vanhatalo A, Kadach S, Wylie LJ, Fulford J, Fergu- son SK, et al. Discrete physiological effects of beetroot juice and potassium nitrate supplementation following 4-wk sprint interval J Appl Physiol. 2018;124(6):1519–28.
- Santana J, Madureira D, de Franca E, Rossi F, Rodrigues B, Fukushima A, et al. Nitrate supplementation combined with a running training program improved time-trial performance in recreationally trained runners. Sports (Basel). 2019. https://doi. org/10.3390/sports7050120.
- Finkel A, Röhrich MA, Maassen N, Lützow M, Blau LS, Hanff E, et al. Long-term effects of NO3− on the relationship between oxygen uptake and power after 3 weeks of supplemented HIHV training. J Appl Physiol. 2018. https://doi.org/10.1152/japplphysi00176.2018.
- Jonvik KL, Nyakayiru J, Pinckaers PJ, Senden JM, van Loon LJ, Verdijk LB. Nitrate-rich vegetables increase plasma nitrate and nitrite concentrations and lower blood pressure in healthy adults. J Nutr. 2016;146(5):986–93. https://doi.org/10.3945/116.229807.
- Wootton-Beard PC, Ryan L. Combined use of multiple methodologies for the measurement of total antioxidant capacity in UK commercially available vegetable juices. Plant Foods Hum Nutr. 2012;67(2):142–7.
- Wylie LJ, Mohr M, Krustrup P, Jackman SR, Ermiotadis G, Kelly J, et al. Dietary nitrate supplementation improves team sport- specific intense intermittent exercise performance. Eur J Appl Physiol. 2013;113(7):1673–84. https://doi.org/10.1007/s0042 1-013-2589-8.
- Bergh U, Thorstensson A, Sjodin B, Hulten B, Piehl K, Karlsson J. Maximal oxygen uptake and muscle fiber types in trained and untrained humans. Med Sci Sports. 1978;10(3):151–4.
- Foster C, Costill DL, Daniels JT, Fink WJ. Skeletal muscle enzyme activity, fiber composition and VO2max in relation to distance running performance. Eur J Appl Physiol Occup Physiol. 1978;39(2):73–80.
- Sahl RE, Morville T, Kraunsoe R, Dela F, Helge JW, Larsen S. Variation in mitochondrial respiratory capacity and myosin heavy chain composition in repeated muscle biopsies. Anal Biochem. 2018;556:119–24. https://doi.org/10.1016/j.ab.2018.06.029.
- Roberts LD, Ashmore T, McNally BD, Murfitt SA, Fernandez BO, Feelisch M, et al. Inorganic nitrate mimics exercise- stimulated muscular fiber-type switching and myokine and γ-aminobutyric acid release. Diabetes. 2017;66(3):674–88.
- Wylie LJ, Ortiz de Zevallos J, Isidore T, Nyman L, Vanhatalo A, Bailey SJ, et al. Dose-dependent effects of dietary nitrate on the oxygen cost of moderate-intensity exercise: acute vs. chronic supplementation. Nitric Oxide. 2016;57:30–9. https://org/10.1016/j.niox.2016.04.004.
- Piknova B, Park JW, Swanson KM, Dey S, Noguchi CT, Schech- ter AN. Skeletal muscle as an endogenous nitrate reservoir. Nitric 2015;47:10–6.
- Coggan AR, Broadstreet SR, Mikhalkova D, Bole I, Leibowitz JL, Kadkhodayan A, et al. Dietary nitrate-induced increases in human muscle power: high versus low responders. Physiol Rep. https://doi.org/10.14814/phy2.13575.
- Kent GL, Dawson B, Cox GR, Abbiss CR, Smith KJ, Croft KD, et al. Effect of dietary nitrate supplementation on thermoregulatory and cardiovascular responses to submaximal cycling in the heat. Eur J Appl Physiol. 2018;118(3):657–68. https://doi. org/10.1007/s00421-018-3809-z.
- Jones AM, Ferguson SK, Bailey SJ, Vanhatalo A, Poole DC. Fiber type-specific effects of dietary nitrate. Exerc Sport Sci Rev. 2016;44(2):53–60. https://doi.org/10.1249/JES.0000000000000074.
- Pingitore A, Lima GP, Mastorci F, Quinones A, Iervasi G, Vassalle C. Exercise and oxidative stress: potential effects of antioxidant dietary strategies in sports. Nutrition. 2015;31(7– 8):916–22. https://doi.org/10.1016/j.nut.2015.02.005.
- Moopanar TR, Allen DG. Reactive oxygen species reduce myofibrillar Ca2+ sensitivity in fatiguing mouse skeletal muscle at 37 C. J Physiol. 2005;564(1):189–99.
- Gomez-Cabrera M-C, Domenech E, Viña J. Moderate exercise is an antioxidant: upregulation of antioxidant genes by training. Free Radic Biol Med. 2008;44(2):126–31.
- Gomez-Cabrera MC, Borras C, Pallardo FV, Sastre J, Ji LL, Vina J. Decreasing xanthine oxidase-mediated oxidative stress prevents useful cellular adaptations to exercise in rats. J Physiol. 2005;567(Pt 1):113–20. https://doi.org/10.1113/jphys2004.080564.
- Irrcher I, Ljubicic V, Hood DA. Interactions between ROS and AMP kinase activity in the regulation of PGC-1α tran- scription in skeletal muscle cells. Am J Physiol Cell Physiol. 2009;296(1):C116–23.
- Merry TL, Ristow M. Do antioxidant supplements interfere with skeletal muscle adaptation to exercise training? J Physiol. 2016;594(18):5135–47.
- Slattery KM, Dascombe B, Wallace LK, Bentley DJ, Coutts AJ. Effect of N-acetylcysteine on cycling performance after intensified training. Med Sci Sports Exerc. 2014;46(6):1114–23. https://doi.org/10.1249/MSS.0000000000000222.
- McKenna MJ, Medved I, Goodman CA, Brown MJ, Bjork- sten AR, Murphy KT, et al. N-acetylcysteine attenuates the decline in muscle Na+, K+-pump activity and delays fatigue during prolonged exercise in humans. J Physiol. 2006;576(Pt 1):279–88. https://doi.org/10.1113/jphysiol.2006.115352.
- Gómez-Cabrera M-C, Pallardó FV, Sastre J, Viña J, García- del-Moral L. Allopurinol and markers of muscle damage among participants in the Tour de France. JAMA. 2003;289(19):2503–4.
- Ichinose T, Nomura S, Someya Y, Akimoto S, Tachiyashiki K, Imaizumi K. Effect of endurance training supplemented with green tea extract on substrate metabolism during exercise in humans. Scand J Med Sci Sports. 2011;21(4):598–605. https://org/10.1111/j.1600-0838.2009.01077.x.
- Borra MT, Smith BC, Denu JM. Mechanism of human SIRT1 activation by resveratrol. J Biol Chem. 2005;280(17):17187–95. https://doi.org/10.1074/jbc.M501250200.
- Gomez-Cabrera MC, Salvador-Pascual A, Cabo H, Ferrando B, Viña J. Redox modulation of mitochondriogenesis in exercise. Does antioxidant supplementation blunt the benefits of exercise training? Free Radic Biol Med. 2015;86:37–46.
- Tappel A. Vitamin E as the biological lipid antioxidant. Vitam Horm. 1962;20:493–510. https ://doi.org/10.1016/S0083-6729(08)60732-3.
- Padayatty SJ, Katz A, Wang Y, Eck P, Kwon O, Lee J-H, et al. Vitamin C as an antioxidant: evaluation of its role in disease J Am Coll Nutr. 2003;22(1):18–35.
- Sharman IM, Down MG, Sen RN. The effects of vitamin E and training on physiological function and athletic performance in adolescent swimmers. Br J Nutr. 1971;26(2):265–76.
- Lawrence JD, Bower RC, Riehl WP, Smith JL. Effects of alpha- tocopherol acetate on the swimming endurance of trained swim- mers. Am J Clin Nutr. 1975;28(3):205–8. https://doi.org/10.1093/ ajcn/28.3.205.
- Rokitzki L, Logemann E, Huber G, Keck E, Keul J. alpha- Tocopherol supplementation in racing cyclists during extreme endurance training. Int J Sport Nutr. 1994;4(3):253–64.
- Oostenbrug G, Mensink R, Hardeman M, De Vries T, Brouns F, Hornstra G. Exercise performance, red blood cell deformability, and lipid peroxidation: effects of fish oil and vitamin E. J Appl 1997;83(3):746–52.
- Gomez-Cabrera MC, Domenech E, Romagnoli M, Arduini A, Borras C, Pallardo FV, et al. Oral administration of vitamin C decreases muscle mitochondrial biogenesis and hampers train- ing-induced adaptations in endurance performance. Am J Clin 2008;87(1):142–9. https://doi.org/10.1093/ajcn/87.1.142.
- Braakhuis AJ, Hopkins WG, Lowe TE. Effects of dietary anti- oxidants on training and performance in female runners. Eur J Sport Sci. 2014;14(2):160–8. https://doi.org/10.1080/174612013.785597.
- Roberts LA, Beattie K, Close GL, Morton JP. Vitamin C consumption does not impair training-induced improvements in exercise performance. Int J Sports Physiol Perform. 2011;6(1):58–69.
- Bryant RJ, Ryder J, Martino P, Kim J, Craig BW. Effects of vita- min E and C supplementation either alone or in combination on exercise-induced lipid peroxidation in trained cyclists. J Strength Cond Res. 2003;17(4):792–800.
- Paulsen G, Cumming KT, Holden G, Hallén J, Rønnestad BR, Sveen O, et al. Vitamin C and E supplementation hampers cellular adaptation to endurance training in humans: a double-blind, randomised, controlled trial. J Physiol. 2014;592(8):1887–901.
- Yfanti C, Akerström T, Nielsen S, Nielsen AR, Mounier R, Mortensen OH, et al. Antioxidant supplementation does not alter endurance training adaptation. Med Sci Sports Exerc. 2010;42(7):1388–95.
- Yfanti C, Nielsen AR, Akerstrom T, Nielsen S, Rose AJ, Rich- ter EA, et al. Effect of antioxidant supplementation on insulin sensitivity in response to endurance exercise training. Am J Physiol Endocrinol Metab. 2011;300(5):E761–70. https://doi. org/10.1152/ajpendo.00207.2010.
- Morrison D, Hughes J, Della Gatta PA, Mason S, Lamon S, Rus- sell AP, et al. Vitamin C and E supplementation prevents some of the cellular adaptations to endurance-training in humans. Free Radic Biol Med. 2015;89:852–62.
- Cumming KT, Raastad T, Holden G, Bastani NE, Schneeberger D, Paronetto MP, et al. Effects of vitamin C and E supplementation on endogenous antioxidant systems and heat shock proteins in response to endurance training. Physiol Rep. 2014;1:1. https://doi.org/10.14814/phy2.12142.
- Ristow M, Zarse K, Oberbach A, Kloting N, Birringer M, Kiehntopf M, et al. Antioxidants prevent health-promoting effects of physical exercise in humans. Proc Natl Acad Sci USA. 2009;106(21):8665–70. https://doi.org/10.1073/pnas.09034 85106.
- Venditti P, Napolitano G, Barone D, Di Meo S. Vitamin E sup- plementation modifies adaptive responses to training in rat skel- etal muscle. Free Radic Res. 2014;48(10):1179–89. https://doi. org/10.3109/10715762.2014.937341.
- Meier P, Renga M, Hoppeler H, Baum O. The impact of anti- oxidant supplements and endurance exercise on genes of the carbohydrate and lipid metabolism in skeletal muscle of mice. Cell Biochem Funct. 2013;31(1):51–9. https://doi.org/10.1002/2859.
- Strobel NA, Peake JM, Matsumoto A, Marsh SA, Coombes JS, Wadley GD. Antioxidant supplementation reduces skeletal muscle mitochondrial biogenesis. Med Sci Sports Exerc. 2011;43(6):1017–24. https://doi.org/10.1249/MSS.0b013e3182 03afa3.
- Higashida K, Kim SH, Higuchi M, Holloszy JO, Han DH. Nor- mal adaptations to exercise despite protection against oxidative stress. Am J Physiol Endocrinol Metab. 2011;301(5):E779–84. https://doi.org/10.1152/ajpendo.00655.2010.
- Kim JC, Park GD, Kim SH. Inhibition of oxidative stress by antioxidant supplementation does not limit muscle mitochondrial biogenesis or endurance capacity in rats. J Nutr Sci Vitaminol (Tokyo). 2017;63(5):277–83.
- Abadi A, Crane JD, Ogborn D, Hettinga B, Akhtar M, Stokl A, et al. Supplementation with alpha-lipoic acid, CoQ10, and vitamin E augments running performance and mitochondrial function in female mice. PLoS One. 2013;8(4):e60722. https://org/10.1371/journal.pone.0060722.
- Asha Devi S, Prathima S, Subramanyam MV. Dietary vitamin E and physical exercise: I. Altered endurance capacity and plasma lipid profile in ageing rats. Exp Gerontol. 2003;38(3):285–90.
- Abbott MJ, Edelman AM, Turcotte LP. CaMKK is an upstream signal of AMP-activated protein kinase in regulation of substrate metabolism in contracting skeletal muscle. Am J Physiol Regul Integr Comp Physiol. 2009;297(6):R1724–32.
- Turcotte LP, Raney MA, Todd MK. ERK1/2 inhibition pre- vents contraction-induced increase in plasma membrane FAT/ CD36 content and FA uptake in rodent muscle. Acta Physiol Scand. 2005;184(2):131–9. https://doi.org/10.1111/j.1365-2005.01445.x.
- Nieman DC, Henson DA, McAnulty SR, McAnulty LS, Mor- row JD, Ahmed A, et al. Vitamin E and immunity after the Kona Triathlon World Championship. Med Sci Sports Exerc. 2004;36(8):1328–35.
- Teixeira VH, Valente HF, Casal SI, Marques AF, Moreira PA. Antioxidants do not prevent postexerciseperoxidation and may delay muscle recovery. Med Sci Sports Exerc. 2009;41(9):1752–60.
- Cobley JN, Close GL, Bailey DM, Davison GW. Exercise redox biochemistry: conceptual, methodological and technical recommendations. Redox Biol. 2017;12:540–8. https://doi. org/10.1016/j.redox.2017.03.022.
- Margaritelis NV, Cobley JN, Paschalis V, Veskoukis AS, Theodorou AA, Kyparos A, et al. Going retro: oxidative stress biomarkers in modern redox biology. Free Radic Biol Med. 2016;98:2–12. https://doi.org/10.1016/j.freeradbio2016.02.005.
- Forman HJ, Augusto O, Brigelius-Flohe R, Dennery PA, Kalyanaraman B, Ischiropoulos H, et al. Even free radicals should follow some rules: a guide to free radical research termi- nology and methodology. Free Radic Biol Med. 2015;78:233–5.
- Somerville V, Bringans C, Braakhuis A. Polyphenols and performance: a systematic review and meta-analysis. Sports Med. 2017;47(8):1589–99. https://doi.org/10.1007/s4027 9-017-0675-5.
- Kulkarni SS, Canto C. The molecular targets of resveratrol. Biochim Biophys Acta. 2015;1852(6):1114–23. https://doi. org/10.1016/j.bbadis.2014.10.005.
- Jiang Q, Cheng X, Cui Y, Xia Q, Yan X, Zhang M, et al. Resveratrol regulates skeletal muscle fibers switching through the Adi- poR1–AMPK–PGC–1α pathway. Food Funct. 2019;10:3334–43.
- Gliemann L, Schmidt JF, Olesen J, Bienso RS, Peronard SL, Grandjean SU, et al. Resveratrol blunts the positive effects of exercise training on cardiovascular health in aged men. J Physiol. 2013;591(20):5047–59. https://doi.org/10.1113/jphys2013.258061.
- Olesen J, Gliemann L, Biensø R, Schmidt J, Hellsten Y, Pilegaard H. Exercise training, but not resveratrol, improves metabolic and inflammatory status in skeletal muscle of aged men. J Physiol. 2014;592(8):1873–86.
- Scribbans TD, Ma JK, Edgett BA, Vorobej KA, Mitchell AS, Zelt JG, et al. Resveratrol supplementation does not augment performance adaptations or fibre-type–specific responses to high- intensity interval training in humans. Appl Physiol Nutr Metab. 2014;39(11):1305–13.
- Skrobuk P, von Kraemer S, Semenova MM, Zitting A, Koistinen HA. Acute exposure to resveratrol inhibits AMPK activity in human skeletal muscle cells. 2012;55(11):3051– 60. https://doi.org/10.1007/s00125-012-2691-1.
- Hart N, Sarga L, Csende Z, Koltai E, Koch LG, Britton SL, et al. Resveratrol enhances exercise training responses in rats selectively bred for high running performance. Food Chem Toxicol. 2013;61:53–9. https://doi.org/10.1016/j.fct.2013.01.051.
- Hart N, Sarga L, Csende Z, Koch LG, Britton SL, Davies KJ,et al. Resveratrol attenuates exercise-induced adaptive responses in rats selectively bred for low running performance. Dose Response. 2014;12(1):57–71. https://doi.org/10.2203/dose-respo13-010.Radak.
- Hodgson AB, Randell RK, Jeukendrup AE. The effect of green tea extract on fat oxidation at rest and during exercise: evidence of efficacy and proposed mechanisms. Adv Nutr. 2013;4(2):129–40.
- Murase T, Haramizu S, Shimotoyodome A, Tokimitsu I, Hase T. Green tea extract improves running endurance in mice by stimu- lating lipid utilization during exercise. Am J Physiol Regul Integr Comp Physiol. 2006;290(6):R1550–6. https://doi.org/10.1152/00752.2005.
- Kuo Y-C, Lin J-C, Bernard JR, Liao Y-H. Green tea extract supplementation does not hamper endurance-training adaptation but improves antioxidant capacity in sedentary men. Appl Physiol Nutr Metab. 2015;40(10):990–6.
- van Loon LJ, Greenhaff PL, Constantin-Teodosiu D, Saris WH, Wagenmakers AJ. The effects of increasing exercise intensity on muscle fuel utilisation in humans. J Physiol. 2001;536(Pt 1):295–304.
- Murase T, Haramizu S, Shimotoyodome A, Nagasawa A, Tokimitsu I. Green tea extract improves endurance capacity and increases muscle lipid oxidation in mice. Am J Physiol Regul Integr Comp Physiol. 2005;288(3):R708–15. https://doi. org/10.1152/ajpregu.00693.2004.
- Dong ZX, Wan L, Wang RJ, Shi YQ, Liu GZ, Zheng SJ, et al. (−)-Epicatechin suppresses angiotensin II-induced cardiac hypertrophy via the activation of the SP1/SIRT1 signaling path- way. Cell Physiol Biochem. 2017;41(5):2004–15. https://doi. org/10.1159/000475396.
- Schwarz NA, Blahnik ZJ, Prahadeeswaran S, McKinley-Barnard SK, Holden SL, Waldhelm A. (−)-Epicatechin supplementation inhibits aerobic adaptations to cycling exercise in humans. Front 2018;5:132. https://doi.org/10.3389/fnut.2018.00132.
- Lee I, Hüttemann M, Kruger A, Bollig-Fischer A, Malek MH. (−)-Epicatechin combined with 8 weeks of treadmill exercise is associated with increased angiogenic and mitochondrial signal- ing in mice. Front Pharmacol. 2015;6:43.
- Wadley GD, Nicolas MA, Hiam D, McConell GK. Xanthine oxidase inhibition attenuates skeletal muscle signaling following acute exercise but does not impair mitochondrial adapta- tions to endurance training. Am J Physiol Endocrinol Metab. 2013;304(8):E853–62.
- Southward K, Rutherfurd-Markwick KJ, Ali A. The effect of acute caffeine ingestion on endurance performance: a systematic review and meta-analysis. Sports Med. 2018. https://doi. org/10.1007/s40279-018-0939-8.
- Lane SC, Areta JL, Bird SR, Coffey VG, Burke LM, Des- brow B, et al. Caffeine ingestion and cycling power output ina low or normal muscle glycogen state. Med Sci Sports Exerc. 2013;45(8):1577–84.
- Beaumont R, Cordery P, Funnell M, Mears S, James L, Watson P. Chronic ingestion of a low dose of caffeine induces tolerance to the performance benefits of caffeine. J Sports Sci. 2017;35(19):1920– 7. https://doi.org/10.1080/02640414.2016.1241421.
- Goncalves LS, Painelli VS, Yamaguchi G, Oliveira LF, Saunders B, da Silva RP, et al. Dispelling the myth that habitual caffeine consumption influences the performance response to acute caf- feine supplementation. J Appl Physiol (1985). 2017;123(1):213– https://doi.org/10.1152/japplphysiol.00260.2017.
- Graham-Paulson T, Perret C, Goosey-Tolfrey V. Improvements in cycling but not handcycling 10 km time trial performance in habitual caffeine users. Nutrients. 2016. https://doi. org/10.3390/nu8070393.
- Lara B, Ruiz-Moreno C, Salinero JJ, Del Coso J. Time course of tolerance to the performance benefits of caffeine. PLoS One. 2019;14(1):e0210275. https://doi.org/10.1371/journpone.0210275.
- Fredholm BB. Astra award lecture. Adenosine, adenosine receptors and the actions of caffeine. Pharmacol Toxicol.1995;76(2):93–101.
- Cole KJ, Costill DL, Starling RD, Goodpaster BH, Trappe SW, Fink WJ. Effect of caffeine ingestion on perception of effort and subsequent work production. Int J Sport Nutr. 1996;6(1):14–23.
- Yeo SE, Jentjens RL, Wallis GA, Jeukendrup AE. Caffeine increases exogenous carbohydrate oxidation during exer- cise. J Appl Physiol (1985). 2005;99(3):844–50. https://doi. org/10.1152/japplphysiol.00170.2005.
- Van Nieuwenhoven MA, Brummer RM, Brouns F. Gastro- intestinal function during exercise: comparison of water, sports drink, and sports drink with caffeine. J Appl Physiol (1985). 2000;89(3):1079–85. https://doi.org/10.1152/jappl.2000.89.3.1079.
- Park S, Scheffler T, Rossie S, Gerrard D. AMPK activity is regu- lated by calcium-mediated protein phosphatase 2A activity. Cell 2013;53(3):217–23.
- Ale-Agha N, Goy C, Jakobs P, Spyridopoulos I, Gonnissen S, Dyballa-Rukes N, et al. CDKN1B/p27 is localized in mitochondria and improves respiration-dependent processes in the cardio- vascular system—new mode of action for caffeine. PLoS Biol. 2018;16(6):e2004408.
- Granata C, Jamnick NA, Bishop DJ. Training-induced changes in mitochondrial content and respiratory function in human skeletal muscle. Sports Med. 2018;48(8):1809–28. https://doi. org/10.1007/s40279-018-0936-y.
- Malek MH, Housh TJ, Coburn JW, Beck TW, Schmidt RJ, Housh DJ, et al. Effects of eight weeks of caffeine supplementation and endurance training on aerobic fitness and body com- position. J Strength Cond Res. 2006;20(4):751–5. https://doi. org/10.1519/R-18345.1.
- Vieira JM, Carvalho FB, Gutierres JM, Soares MSP, Oliveira PS, Rubin MA, et al. Caffeine prevents high-intensity exercise-induced increase in enzymatic antioxidant and Na(+)– K(+)-ATPase activities and reduction of anxiolytic like- behaviour in rats. Redox Rep. 2017;22(6):493–500. https://doi. org/10.1080/13510002.2017.1322739.
- Boyett JC, Giersch GE, Womack CJ, Saunders MJ, Hughey CA, Daley HM, et al. Time of day and training status both impact the efficacy of caffeine for short duration cycling performance. 2016;8(10):639.
- Temple JL, Ziegler AM. Gender differences in subjective and physiological responses to caffeine and the role of steroid hormones. J Caffeine Res. 2011;1(1):41–8. https://doi.org/10.1089/2011.0005.
- Guest N, Corey P, Vescovi J, El-Sohemy A. Caffeine, CYP1A2 genotype, and endurance performance in athletes. Med Sci Sports Exerc. 2018. https://doi.org/10.1249/MSS.0000000000 001596.
- Spriet LL. Exercise and sport performance with low doses of caffeine. Sports Med. 2014;44(Suppl 2):S175–84. https://doi. org/10.1007/s40279-014-0257-8.
- Kreider RB, Kalman DS, Antonio J, Ziegenfuss TN, Wildman R, Collins R, et al. International Society of Sports Nutrition position stand: safety and efficacy of creatine supplementation in exercise, sport, and medicine. J Int Soc Sports Nutr. 2017;14:18. https://org/10.1186/s12970-017-0173-z.
- Harris RC, Soderlund K, Hultman E. Elevation of creatine in resting and exercised muscle of normal subjects by creatine sup- Clin Sci (Lond). 1992;83(3):367–74.
- Green AL, Hultman E, Macdonald IA, Sewell DA, Greenhaff PL. Carbohydrate ingestion augments skeletal muscle creatine accumulation during creatine supplementation in humans. Am J Physiol. 1996;271(5 Pt 1):E821–6. https://doi.org/10.1152/ajpen1996.271.5.E821.
- Wallimann T, Tokarska-Schlattner M, Schlattner U. The cre- atine kinase system and pleiotropic effects of creatine. Amino Acids. 2011;40(5):1271–96. https://doi.org/10.1007/s0072 6-011-0877-3.
- Kuznetsov AV, Tiivel T, Sikk P, Kaambre T, Kay L, Daneshrad Z, et al. Striking differences between the kinetics of regulation of respiration by ADP in slow-twitch and fast-twitch muscles in vivo. Eur J Biochem. 1996;241(3):909–15.
- Rahimi R. Creatine supplementation decreases oxidative DNA damage and lipid peroxidation induced by a single bout of resistance exercise. J Strength Cond Res. 2011;25(12):3448–55. https://doi.org/10.1519/JSC.0b013e3182162f2b.
- Tomcik KA, Camera DM, Bone JL, Ross ML, Jeacocke NA, Tachtsis B, et al. Effects of creatine and carbohydrate loading on cycling time trial performance. Med Sci Sports Exerc. 2018;50(1):141–50. https://org/10.1249/MSS.0000000000001401.
- Kendall KL, Smith AE, Graef JL, Fukuda DH, Moon JR, Beck TW, et al. Effects of four weeks of high-intensity interval train- ing and creatine supplementation on critical power and anaero- bic working capacity in college-aged men. J Strength Cond Res. 2009;23(6):1663–9. https://doi.org/10.1519/JSC.0b013e3181 b1fd1f.
- Graef JL, Smith AE, Kendall KL, Fukuda DH, Moon JR, Beck TW, et al. The effects of four weeks of creatine supplementation and high-intensity interval training on cardiorespiratory fitness: a randomized controlled trial. J Int Soc Sports Nutr. 2009;6:18. https://doi.org/10.1186/1550-2783-6-18.
- Forbes SC, Sletten N, Durrer C, Myette-Côté É, Candow D, Little JP. Creatine Monohydrate supplementation does not augment fit- ness, performance, or body composition adaptations in response to four weeks of high-intensity interval training in young females. Int J Sport Nutr Exerc Metab. 2017;27(3):285–92.
- McCracken M, Ainsworth B, Hackney AC. Effects of the menstrual cycle phase on the blood lactate responses to exercise. Eur J Appl Physiol Occup Physiol. 1994;69(2):174–5.
- Chwalbinska-Moneta J. Effect of creatine supplementation on aerobic performance and anaerobic capacity in elite rowers in the course of endurance training. Int J Sport Nutr Exerc Metab. 2003;13(2):173–83.
- Nelson AG, Day R, Glickman-Weiss EL, Hegsted M, Kokkonen J, Sampson B. Creatine supplementation alters the response to a graded cycle ergometer test. Eur J Appl Physiol. 2000;83(1):89– https://doi.org/10.1007/s004210000244.
- Maughan RJ. Contamination of dietary supplements and positive drug tests in sport. J Sports Sci. 2005;23(9):883–9. https://doi. org/10.1080/02640410400023258.
- Shill DD, Southern WM, Willingham TB, Lansford KA, McCully KK, Jenkins NT. Mitochondria-specific antioxidant supplementation does not influence endurance exercise train- ing-induced adaptations in circulating angiogenic cells, skeletal muscle oxidative capacity or maximal oxygen uptake. J Physiol. 2016;594(23):7005–14.
- Polley KR, Jenkins N, O’Connor P, McCully K. Influence of exercise training with resveratrol supplementation on skeletal muscle mitochondrial capacity. Appl Physiol Nutr Metab. 2016;41(1):26–32. https://doi.org/10.1139/apnm-2015-0370.
- Dolinsky VW, Jones KE, Sidhu RS, Haykowsky M, Czubryt MP, Gordon T, et al. Improvements in skeletal muscle strength and cardiac function induced by resveratrol during exercise training contribute to enhanced exercise performance in rats. J Physiol. 2012;590(11):2783–99. https://doi.org/10.1113/jphys2012.230490.
- Kan NW, Ho CS, Chiu YS, Huang WC, Chen PY,Tung YT, et al. Effects of resveratrol supplementation and exercise training on exercise performance in middle-aged mice. Molecules. 2016. https://doi.org/10.3390/molecules21050661.


